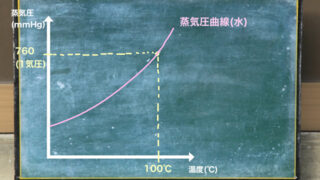
前回の記事では質量モル濃度の公式について解説しました。
「質量モル濃度を利用する場合の一つに、蒸気圧降下度を求める場合がありますよ」
という説明をして終わっています。
⇒質量モル濃度の公式
そもそも蒸気圧降下とはどんな現象なのでしょう?
わかりやすく解説していきたいと思います。
蒸気圧降下とは?わかりやすく説明
蒸気圧降下とはわかりやすく簡単にいうと『蒸発しにくくなる』ということです。

海水で濡れた水着と純粋で濡れた水着を同時に乾かしたとしましょう。
この場合、海水で濡れた水着と純粋で濡れた水着だと
海水で濡れた服の方が乾燥しにくいです。
海水で濡れた水着の方が乾燥するのに時間がかかるということです。
海水の方が蒸発しにくいからです。
海水というのは溶質(塩)が水という溶媒に溶けた水溶液の状態です。
⇒溶媒・溶質・溶液の違いをわかりやすく例を挙げて解説
逆に純水というのはただの水です。
化学的にいったら溶媒100%が純粋です。
純水の方が蒸発しやすく、溶質(塩)が入った水溶液にすると
ちょっと蒸発が起こりにくくなります。
この現象のことを蒸気圧降下といいます。
そして蒸気圧降下が起こると沸点が上がります。
蒸気圧降下が起こると沸点が上がる理由については次の記事で解説します。
今回は蒸気圧降下について図を使ってもっとわかりやすく解説していきますね。
蒸気圧降下が起こる理由をわかりやすく解説
塩などが溶けた水溶液はただの水(純水)よりも蒸発しにくくなるメカニズムについて
説明してみたいと思います。
以下の図は同じ大きさのビーカーの中に純水と水溶液(塩入り)が入っているとしましょう。

左の図はただの水(純水、真水)で溶媒(水)、
右の図は塩という溶質が溶けた水溶液だとしましょう。
何が違うか?水面(表面)に注目してください。
純水は水分子か水面にありません。
上記左側の図では水面に溶媒(水分子)が100個あるとしましょう。
右側の図(水溶液)の表面にも分子を並べます。
ただ水溶液というのは当然、溶質(塩)を含んでいるので
水面にも溶質分子(塩)が入り込んできます。

なので、右側の図では水面に100個中40個が溶質分子で、
60個が溶媒分子が存在するとしましょう。
では蒸発という現象について考えてみましょう。
蒸発というのは水面から気体となって出ていく現象のことです。
水面の水分子(溶媒)が気体となって外に出ていく現象こそが蒸発になります。
今、左の図も右の図も合計で100個の分子が水面に並んでいます。
ここで条件を作ります。
水面に並んでいる分子のうち100個の分子のうち50個の分子、
つまり2分の1の確率で気体になれるとする。
この場合、純水で蒸発できる分子の数は50個となりますね。
100個÷2=50個です。
すると以下のような図になりますね。
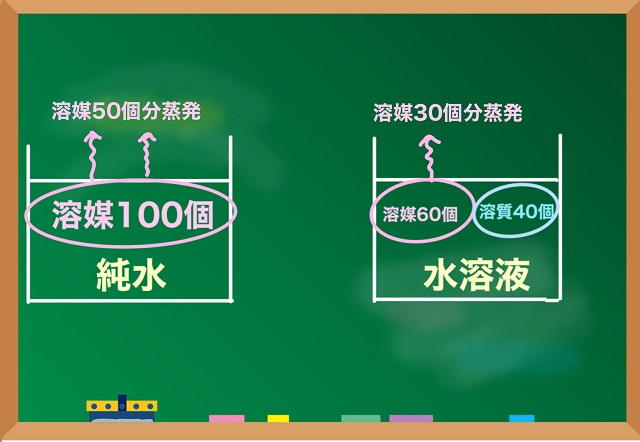
右側の図だと60個の溶媒のうち半分の30個が蒸発するわけです。
溶質(塩)は蒸発しませんから。
この辺は中学校の理科で食塩水の濃度の問題を解いたことがある方なら
わかっていただけるでしょう。
どうですか?
純水(真水)と水溶液を比較してどちらの方が蒸発して出ていく水蒸気の量が多いですか?
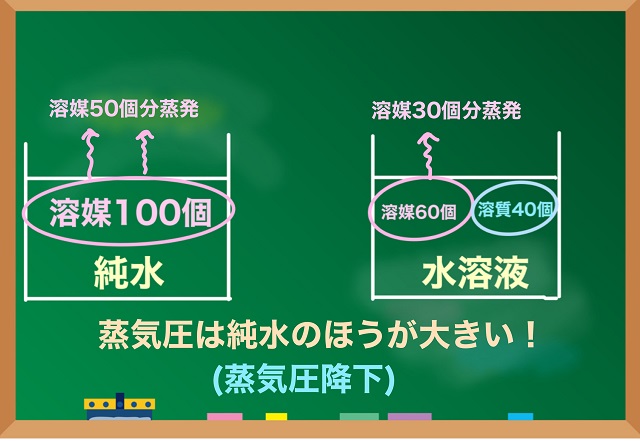
結論としては左側の真水(純水)の図の方が蒸発している水蒸気の量が多いですよね。
一定時間あたりに蒸発する量は純水の方が多く、
水溶液になると、溶質を溶かした分だけ少なくなるのがわかりますね。
溶質(塩)が入り込んだ分だけ、
蒸発可能な分子(溶媒)の数が減ってしまうからです。
つまり、蒸発してできた水蒸気の圧力は
明らかに左側の純水(真水)の方が大きくなりますね。
なので、右側の図が仮に海水だとすると
海水の方が蒸発しにくいから干しても、渇きが悪いのです。
この現象のことを蒸気圧降下と読んでいて、
同時に蒸気圧降下が起こる理由にもなっています。
溶質が入り込むことで蒸発が起こりにくくなる、
なぜなら蒸発できる分子の数が減ってしまうからです。
これが蒸気圧降下です。
蒸気圧降下が起きたら沸点が上がりますが
理由については次の記事で解説します。
⇒沸点上昇が起こる理由(ヒント蒸気圧降下)