「溶媒、溶質、溶液のの違いが分かりません・・・」という方が多いです。
確かに溶媒も溶質も溶液もどれも頭文字に『溶』の文字がついているので
違いがよくわからなくなりますよね。
でも心配無用です。
安心してください。
今回の記事では溶媒、溶質、溶液の違いがよくわかるように
例を挙げながらわかりやすく解説していきますね。
溶媒、溶質、溶液の違い
溶液とは溶媒と溶質を混ぜたもののこと。
溶液=溶媒+溶質
です。

たとえば、溶媒が水で溶質が塩だとすると
混ぜると食塩水になりますが、この食塩水が溶液です。
溶媒(水)+溶質(塩)=溶液(食塩水)
ということです。
・溶質・・・液体に溶けている物質(例:塩)
・溶媒・・・溶質を溶かす液体のこと(例:水)
・溶液・・・溶質が溶媒に溶けた液体全体(例:食塩水)
ということです。
溶媒、溶液、溶質それぞれ頭文字に『溶』という文字がついています。
この『溶』には固体が液体になるというような意味があるのです。
『溶』は『溶ける(とける)』とか『溶かす(とかす)』と日本語で表現することがありますよね。
たとえば食塩が水に溶かされて食塩水になります。
・溶質・・・食塩水における食塩みたいに水などの溶媒に溶けている物質
・溶媒・・・食塩水みたいに出来上がった溶液のもとになった液体(多くは水)
・溶液・・・溶媒と溶質によってできた液体(食塩水)
ということです。
・溶質・・・溶ける方の物質のこと
・溶媒・・・溶かす方の液体のこと
・溶液・・・固体液体気体が溶けてできた均一な混合物のこと
つまり、溶媒と溶質を混ぜてできた混合物のことを溶液と呼ぶのです。
ちなみに
溶媒になるものは水だけではありません。
たとえば有機溶媒なんかも溶媒になります。
有機物が溶媒になることもありますから。
とにかく溶かす方の液体のことを溶媒といいます。
たとえば、果実酒。
・溶質は砂糖と果実(果物)
・溶媒はアルコール
・溶液は果実酒
となります。
たとえば、食塩水だったら塩が溶質で溶媒が水、
食塩水が溶液になります。
・砂糖が溶質
・水が溶媒
・砂糖水が溶液
になります。
溶媒と溶質をさらに細かく分類してみると・・・
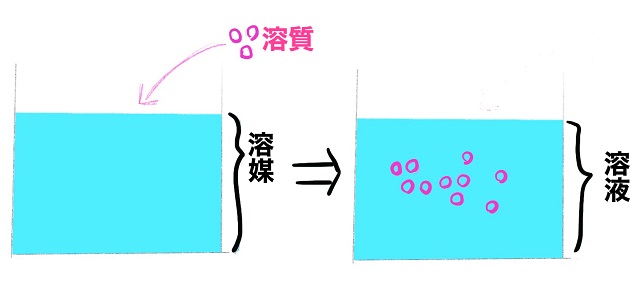
ビーカーの中に水を入れました。
ここまでの解説で分かりますよね。
この水は溶媒です。
そしてこの溶媒(水)の中に塩や砂糖などの粒を溶かします。
この溶かす粒のことを溶質といいます。
ここまでは大丈夫ですよね。
そして溶媒に溶質が溶けると
溶液になるわけですよ。
まずは溶媒、溶質、溶液の違いが理解できているか?
再確認してくださいね。
そして溶媒の中には以前解説しましたが
極性分子からできている溶媒、具体的には水みたいなやつ。
これを極性溶媒といいます。
極性についてはこちらの記事で詳しく解説しています。
⇒電気陰性度と極性についてわかりやすく解説
この記事をご覧のあなたは極性溶媒の具体例として
水を覚えておきましょう。
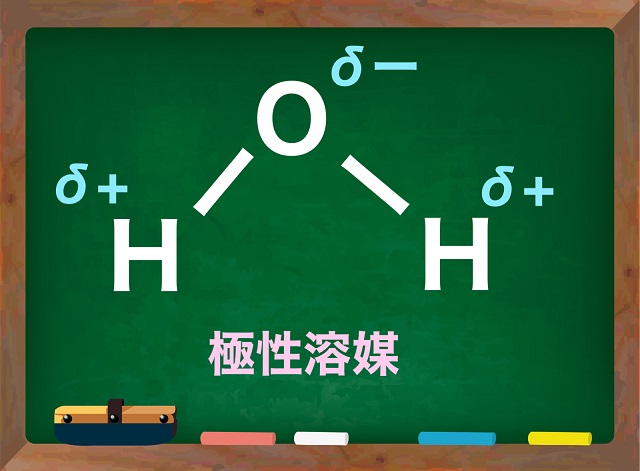
水は折れ線型でδ+(デルタプラス)、
δー(デルタマイナス)に分極していて
分子全体でも極性が残ってしまう極性分子です。
⇒極性と水素結合ってどんな関係?
⇒極性分子とは?簡単にわかりやすく解説
この極性分子からできている溶媒を極性溶媒といいます。
これに対して無極性分子から出来上がっている溶媒を
無極性溶媒といいます。
無極性溶媒の具体例はベンゼンが該当します。
今後ベンゼンという名前はよく聞くことになるので
無極性溶媒の代表例としてベンゼンを覚えておきましょう。
ベンゼンは分子式、$C_6H_6 $と書きます。
⇒ベンゼンの構造式の謎を解決!|ケクレ構造や非局在化についても解説
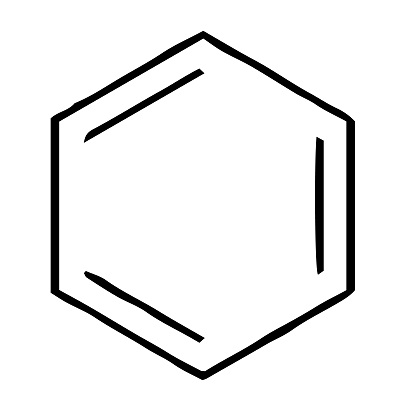
また$C_6H_6 $のベンゼンは上記のように書くこともあります。
正六角形の中に棒を三本引きます。
形は見慣れておきましょう。
・極性溶媒
・無極性溶媒
また溶質の中には極性溶媒に溶かして
陽イオンと陰イオンに電離する電解質と呼ばれるものがあります。
電解質はプラスとマイナスに分かれます。
⇒電解質と非電解質の見分け方
⇒電解質と非電解質の違いと例
覚えておいて欲しい電解質としてはNaCl(食塩)があります。
NaClを水に溶かすと$Na^{+} $と$Cl^{ー} $に電離します。
あとは極性溶媒に溶かしても
電離しない非電解質というものがあります。
⇒電離度覚えるべきもの一覧と公式について解説
そして非電解質として覚えておいて欲しいのはグルコース(ブドウ糖)です。
ブドウ糖は$C_6H_12O_6 $と書きます。
・電解質(具体例は食塩)
・非電解質(具体例はブドウ糖)
あなたが化学を勉強していく中で
食塩とブドウ糖はよく見かけることがあると思います。
なので少しずつ慣れていきましょう。
以上で解説を終わりたいと思います。
溶媒と溶質と溶液の違いについて
例を挙げながら、いろんな角度からかなり噛み砕いて
わかりやすく解説したつもりです。
この記事が参考になったという方は
ぜひブックマークしておいていただけるとうれしいです。
これからも化学的な内容をわかりやすく解説していきたいと思いますので
よろしくお願いします。