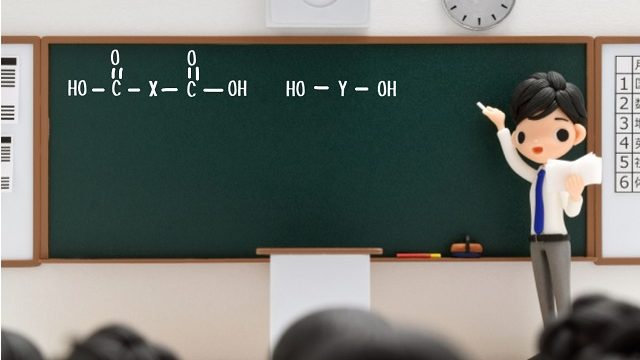水って0℃になったら凍りますよね。
そこまではほとんどの方が知っている話だと思います。
では以下の話は知ってますか?
ただの水よりも水溶液の方が
凍りにくいという事実です。
確かに塩化ナトリウム水溶液は水よりも凍りにくいけど、果たしてどれほどの効果があるんだろうか
— てりあ (@material_1024) January 24, 2012
「どうして?」
と疑問に感じる方もいるかもしれません。
凝固点降下という化学の話が絡んでくるので
ちょっとややこしい話になります。
そこでこの記事では凝固点降下の原理について解説していきます。
そして凝固点降下の原理が働いている身近な例もご紹介します。
Contents
凝固点降下の原理
水が氷る温度を凝固点といいます。
そして水が氷る温度というのは通常0℃です。
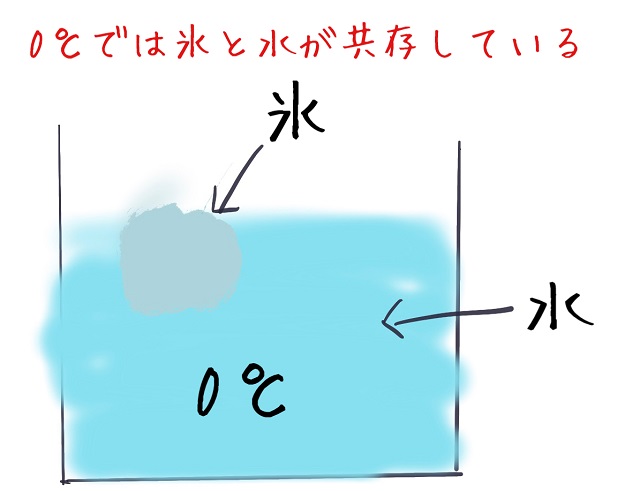
0℃で氷るわけですが、
ただ0℃では氷と水が共存しています。
厳密には、水は0°Cで凍る訳ではないはず。
0°Cは、水(液体)と氷(固体)が共存できる、
矛盾した温度だったはず。— ぞんぽた@C101 2日目 東Q-03b売り子 (@zonepotage) April 20, 2015
気温が0℃付近の日にノーマルタイヤで運転するのは自殺行為なんですよね
タイヤの接地面に水と氷が共存するだけで簡単に設置力を失って車が浮くので
— 天城 (@Amagi45010626) December 23, 2022
ところで氷ってコップの水の中に入れると
プカーッと浮きますよね。
ということは凝固点の状態というのは
氷と水が共存しているということになりますよね。
・水が氷る温度を凝固点で、0℃が該当する
・0℃は水と氷が共存している
・ということは凝固点では水と氷が共存している
ということです。
で、氷が解けるスピードと
水が氷るスピードが一緒の状態、
これが普段、私たちが生活している状態の凝固点です。
たとえば北海道に行ったとしましょう。
網走の方に流氷が流れ着くという話を
テレビでよくやってますよね。
2022年の旅行 3月
知床(流氷ウォーク)、網走 pic.twitter.com/TjYMYTFLBw— ポッペ@アイカツ10thライブ (@poppe51) January 2, 2023
その流氷を拾ってきたとしましょう。
表面をきれいに洗って割ったとします。
割った流氷の真ん中部分を舐めたらどんな味がすると思いますか?
一応海にある氷だからしょっぱい味がしそうですね。
でもしょっぱくありません。
これは流氷んとこにキャンプした(流氷上ではない)時の写真。日没直後です。翌日、流氷をかち割って、流氷ロックでウイスキー。めちゃ美味。よくしょっぱくないの?って聞かれますが、海水は凍りません。アムール川からドンブラコって流れてきた純真水です。 pic.twitter.com/hWXXpEmS2O
— 平野勝之 (@hiranokatsuyuki) November 12, 2016
つまり海の水が氷るときには
塩を含んだ形では氷らないということです。
水だけが氷っていきます。
流氷の真ん中をなめてもしょっぱくないのです。
水溶液の場合には
溶質が溶けているわけですよね。
ただ砂糖や塩は氷の中には含まれません。
するとこの氷と砂糖や塩の水溶液が共存している状態というのは
溶質(砂糖や塩のこと)が水に溶けているので
氷る勢いというのが弱いのです。
溶質が邪魔します。
水が氷になろうかなというところに
溶質が邪魔してくるのです。
くどいようですが砂糖や塩といった溶質は氷の中には含まれませんからね。
でも、氷が水になる場合、
氷の中には溶質といった邪魔者はいません。
すると氷は水になりやすいです。
するとこのままだとどんどん氷が水に解ける量の方が
水が氷になる量よりも多いわけです。
このままだとどんどん氷が解けてしまいます。
どうすればよいでしょう?
もう少し温度を下げて水が氷になるスピードを
上げてあげないといけません。
ということで温度を下げる必要があるわけです。
温度を下げることによって凝固するスピードと
解けるスピードを一緒にしてあげるということです。
ということで温度を下げて氷と水溶液を共存させることができます。
つまり凝固点が下がる(降下する)ということです。
このように水に砂糖や塩といった溶質を溶かすと
凝固する温度が下がるのです。
これを凝固点降下といいます。
凝固点降下の原理が働いている身近な例
凝固点降下の原理を利用した身近な例には何があるでしょう?
エチレングリコールを主成分とした不凍液を挙げることができます。
自動車の冷却水が凍らないようにするためのものです。
車に興味のない方はよくわからないかもしれませんが、
車の中には冷却水というものがあります。
やべえって俺が乗ってた車冷却水ばちもれオーバーヒート寸前(くっそ市内で交通量多いところ)
メーター見て気づいてボンネットあけて良かった、こんなとこでオバヒしたら事故って死ぬ pic.twitter.com/NseUDk8w49— GeKkA (@GeKkA__RaIMeI__) January 7, 2023
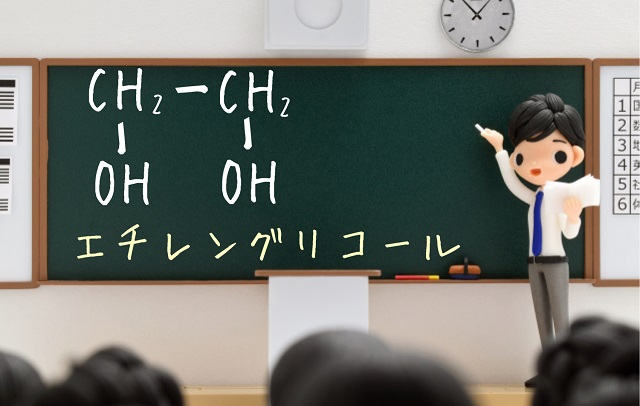
冷却水のところにエチレングリコールを主成分とした不凍液を入れます。
ちなみにエチレングリコール自体を人間や動物が舐めると下痢になったりしますので
絶対に口に入れないようにお願いします。
ラジエーターの不凍液も緑にしてあってエチレングリコール入ってるから
車の下とかで漏れてるところに入り込んだ猫ちゃんが舐めて緑色のゲロと下痢をしてたりする— 呼吸 (@ebiflyyyyyyyy) March 17, 2021
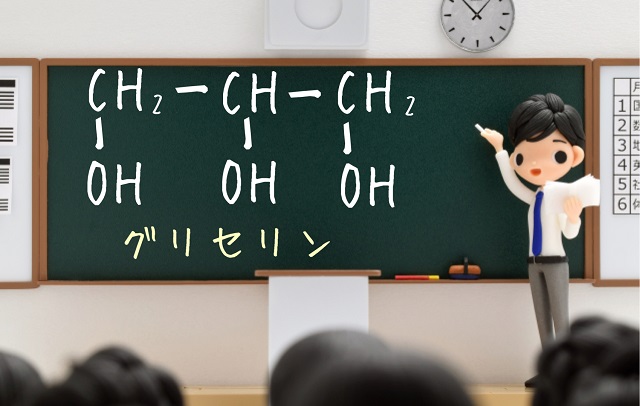
エチレングリコールの構造式にCHとOHを加えると
グリセリンになります。
このグリセリンは歯磨き粉に利用されることが昔ありました。
グリセリンは甘味があるので、甘味を足すために歯磨き粉に利用されていたのです。
@tk13sg 冷却水はな。エチレングリコールって成分が入っててな。昔の歯磨き粉とかの甘味料に使われててだな…
— たかだは静かに暮らしたい。 (@tkd_373rr) September 8, 2015
歯磨き粉作り🌿#重曹 #グリセリン #エッセンシャル
を混ぜるだけ〜♪超簡単!おいしい優しいサイコ〜ウ✨🌏 pic.twitter.com/C12tcd00pF— 森暮らしNICO (@mori_nico8) December 10, 2021
でも間違ったのか故意なのか
歯磨き粉の中にグリセリンでなくエチレングリコールが入っていて
死者が出るという騒動がありました。
エチレングリコールって何年か前に中国がグリコールより安価だからと歯磨き粉に代用して大勢死人出なかったっけ
— とぉ@黒シャツ (@kuro_shatty_t) July 31, 2012
以上のようにエチレングリコールは体に悪いのですが、
もう1つCHとOHがくっついたグリセリンになると問題はなくなります。
話を元に戻して自動車にエチレングリコールが入っても問題ありませんから
エチレングリコールが利用されているわけです。
このように書くと、「でも別にグリセリンでいいんじゃない!?
その方が安全性が高いんだし」って思った方もいるかもしれませんね。
でも、エチレングリコールの方がグリセリンよりも
仕入れ価格が安いのです。
私は獣医師として動物病院を運営しているからわかるのですが、
犬猫の下剤としてグリセリンを使うこともあります。
業者から仕入れるときに価格の違いを実感します。
我が家のおデブ猫が5日間便秘で苦しんで食欲も落ちてゲロゲロ〜の日々。ご飯を変えてしまった私のせいなので、毎日朝晩お腹マッサージしたりグリセリン浣腸したり頑張ってやっとやっと昨日解放されたー😭みんなで拍手したくらい嬉しかったよー👏ごめんねごめんねと平謝りで前のご飯に戻しましたー
— まーべらす𓃰 (@nyancoo520) September 16, 2020
とにかく車にエチレングリコールを利用するのは
グリセリンよりもコストが安いからです。
コストの安いエチレングリコールを水に溶かして
冷却水として利用されています。
ただの蒸留水を冷却水として利用していると
たとえば真冬の北海道旅行中に凍ってしまうでしょう。
氷になると体積が増えます。
破裂する可能性があるので大変危険です。
薄いガラスのコップに水を入れて冷凍庫に入れないはず。
体積の大きい氷になりコップが割れてしまうからです。
おはサンユウ🙌
天気は☀️「水分は固まる(氷になる)と体積が増える」というのを理科の実験でやったのを覚えていますか❓
これは屋根や壁の内部でも起こります!!
寒い日が続くので、要注意⚠️
雨漏りの原因にもなるので屋根や外壁のヒビ割れは放置せずに直しましょう。今日も1日頑張りましょう💪 pic.twitter.com/3hFJVzJ2mp
— 豊川・蒲郡のサンユウ(参邑)外壁塗装・リフォーム、お家のことならお任せ (@sanyu33toyokawa) January 20, 2022
だから凍らないように凝固点を下げるために
エチレングリコールを溶かして水溶液にして利用しているのです。
これは凝固点降下の原理を利用しています。
これと同様に
凍結防止剤も凝固点降下の原理を利用しています。
⇒KYK 凍結防止剤メタブルー ポリ缶タイプ 20L 寒さ対策用品 1点
路上の凍結を防ぐために$CaCl_2 $(塩化カルシウム)をまくことがあります。
凍結防止の塩化カルシウムを撒きまくった島根と広島の山道とか中国道走ってたから、車が真っ白に。
朝から洗車したら、フロントガラスに飛石で小さなヒビ。
昨日走行中にガラスになんか当った音は聞いている。とりあえず、補修剤入荷待ち。 pic.twitter.com/6U7myjWxgQ
— MOOMIN PAPA (@moominpapa1967) January 4, 2023
路上が凍結するといったらかなり寒い地方になるかと思います。
特に盆地の長野県とか山梨県とか。
$CaCl_2 $(塩化カルシウム)を凍りそうなところに散布するわけです。
すると$CaCl_2 $(塩化カルシウム)というのは
溶質が溶けて凝固点を下げることができて
道路が凍らないようにある程度防ぐことができます。
道路が凍って滑るのは危ないですからね。

特に橋は危ないです。
橋は吹きっさらしのことが多いです。
するとものすごく冷えます。
特に橋のつなぎ目のところには金属を入れてます。
底の部分が凍ってタイヤが空回りするとスリップ事故を起こす危険性があります。
そういったことを防止するために$CaCl_2 $(塩化カルシウム)といった凍結防止剤が存在します。
なので$CaCl_2 $(塩化カルシウム)といった凍結防止剤は
凝固点降下の具体例になります。
真冬の駅のホームで
地面が凍ると、滑ってこけて大けがする危険性があります。
そんな場合に、あらかじめ凍結防止剤をまいておくと
路面が凍結しなくなるので
滑ってこけてケガするリスクを避けることができます。
もう既に凍結防止剤がブチまかれている用意周到な高尾駅近辺。
どうでもいいけど、CaCl2で凝固点降下だったっけ… pic.twitter.com/tlapHE2O52
— 𝕌☆𝔾 (@agoigougo) January 29, 2015
舞浜駅、凍結防止剤散布中。
#TDR_now pic.twitter.com/rUKjw788Oj— プルを (@pluwota) January 22, 2018
以上で解説を終わります。