今回の記事では中和滴定の器具に関して解説します。
ただ最初は中和滴定という文字の意味から考えていきましょう。
文字の意味がわからないとどうして今回解説する器具を使うのか?
よくわからなくなってしまうので。
Contents
中和滴定の目的
中和滴定の目的と原理って自分で考えるの?それともそのままノートのうつす感じ?
— 𝑚𝑖𝑢 (@umiumimiu_tk) May 19, 2021
中和滴定(ちゅうわてきてい)の『滴(てき)』というのは1滴、2滴と
ポタポタ垂らすという意味です。
では中和滴定の目的は何でしょうか?
単に1滴、2滴とポタポタ垂らすだけの話なら目薬を垂らすのも中和滴定になってしまいますからね。
花粉症なんですが使い終わった目薬容器に薄め液入れてます。
1滴2滴、ポタポタって出して皿の上で濃度調整とかにちょうどいいですよ。 pic.twitter.com/aY9ZeJ256I— 泰山府君(再出発) (@new_taizanfukun) June 7, 2019
中和滴定は単に液体をポタポタ垂らすわけではありません。
中和滴定には目的があります。
未知の酸、あるいは塩基が関係します。
ただ未知の酸、あるいじゃ塩基というと
未確認飛行物体に積んである酸とか塩基みたいなイメージを持つ方もいるかもしれませんね。
ですがそうではありません。
未知の酸、塩基というのは『酸や塩基の濃度がわからない』という意味です。
酸や塩基の濃度がわからない(=未知)というときに中和滴定をやって
その濃度を求める
です。
未知とは濃度がわからないという意味になります。
つまり、酸や塩基の濃度がわからないときに
酸の濃度がわからないなら塩基、塩基の濃度がわからないなら酸を加えて中和することによって
濃度を決める方法が中和滴定ということです。
ここまで解説した中和滴定をやる目的を理解しながら以下、
解説を読んでいってくださいね。
中和滴定の器具の名称と使い方
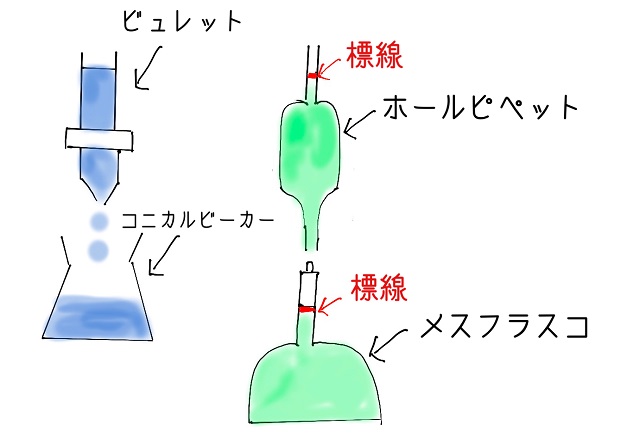
上記図をご覧ください。
左上にあるのがビュレットです。
そしてコニカルビーカーが左下にあります。
ちなみに正式にはコニカルビーカーを使うのですが
代わりに三角フラスコを中和滴定で使ってもOKです。
たとえば酸の濃度がわからないとしましょう。
酸をコニカルビーカーに入れておくわけです。
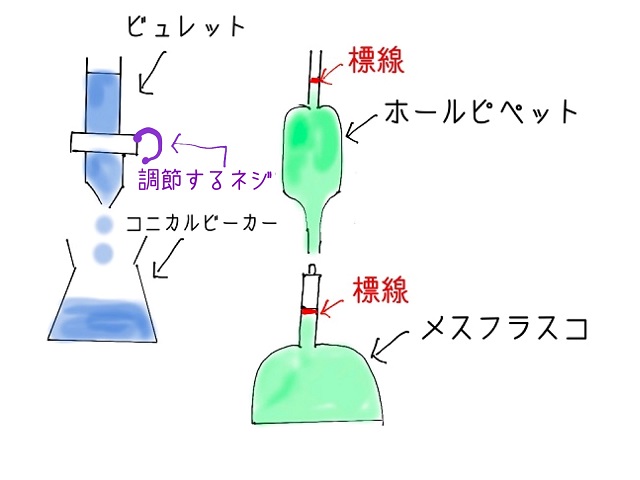
そして濃度がわかっている塩基をビュレットに入れます。
で、ビュレットには調節するネジがついています。
この調節するネジを使ってビュレットに入っている塩基をポタポタとコニカルビーカーに垂らしていきます。
そしてちょうど中和し終わったというところを確認して
どれくらい塩基を使ったかを確認します。
まずは上記器具の名前を覚えてくださいね。
ここまでで解説したのはビュレットとコニカルビーカーです。
今日の1年生は?
バイオ化学実験です🧪
いよいよ中和滴定が始まりました!
ビュレット並べて滴定練習
1人1人滴定練習できるのは
TTCバイオ科のすごさ!滴定のできない学生?
うちにはいません(たぶん)
理由はこちらのブログで↓https://t.co/yMlgFkYzpS#中和滴定 #実験の鬼 pic.twitter.com/cTV0KiBVnN— 専門学校 東京テクニカルカレッジ バイオテクノロジー科 (@TTCbio) June 20, 2022

そのほかにも中和滴定に利用する器具はあります。
上記図の右側の器具です。
上記図の左側の器具は表舞台の器具で
右側の器具は裏舞台の器具といった感じになります。
図の右上はホールピペットです。
あなたが高校生であったり大学生で化学の実験があるなら
おそらくホールピペットを使う機会があるでしょう。
ホールピペットで一般的に多いのは10mL用で
口で酸の溶液などを吸って中和滴定を行います。
私は未だにホールピペットを口で吸うという衝撃が忘れられないんだけど pic.twitter.com/TKT1ZoHQI5
— だひ汁🐄✈️ (@appletaart) September 11, 2020
そしてホールピペットには標線(ひょうせん)がついていて
ここまで入れると10mLのホールピペットならちょうど10mLとなります。
ちなみにホールピペットで標線があるところって細いですよね。
どうして細いと思います?
細いとすぐに変化が出ますが、太いと吸っても吸っても変化しづらいですよね。
細いとちょっと吸っても液体が上昇してきますけど
太いと吸っても液体の上昇が細い場合よりも遅くなりますよね。
とにかくホールピペットは標線のところはすごく細いです。
ボーッとしながら液体を吸うと
あなたの口に入っていってしまいますからね。
ご注意ください。
実験によっては水酸化ナトリウムを吸うこともあります。
そんな危険な液体を吸ってしまうと命にもかかわってしまいます。
なので、中和滴定の実験をするときは真剣勝負でお願いします。

そして上記図の右下にメスフラスコがあります。
メスフラスコにはちゃんと上部にフタがついています。
メスフラスコにはいろんな種類があります。
250mL用、500mL用、1L用などいろいろあります。
メスフラスコも標線がある部分は細いです。
そして標線のある部分まで液体を入れるとピッタリになります。
たとえば500mLのメスフラスコなら標線まで液体を入れることでピッタリ500mLだとわかります。
メスフラスコは何のために使うか?
たとえば、ホールピペットで正確に10mLとるとしましょう。
これをメスフラスコに入れます。
で、水をメスフラスコに加えてピッタリ標線まで(500mL)持ってきます。
つまりメスフラスコは薄めるために使う器具だということです。
ホールピペットは正確に10mLなら10mLという体積をとってくる器具ですが
メスフラスコは薄める器具だということです。
たとえば、ホールピペットで10mLとってきてメスフラスコに入れます。
そのあとホールピペットに水を加えて500mLまで薄める、そんな器具です。
こういうことがわかっていると
ホールピペットやメスフラスコを使いやすいと思います。
中和滴定の器具を準備する際の注意点
それから当然ですが、器具を準備するということが必要です。

どうやって準備すればよいのでしょう?
まずビュレットとホールピペットから。
ビュレットとホールピペットは準備の仕方は同じです。
ではどうやって準備すればよいのでしょう?
たとえば塩酸を入れるとしましょう。
塩酸でビュレットやホールピペットをよくすすぎます。
これが重要です。
つまりホールピペットとビュレットを準備する場合には
中に入れる溶液ですすぐということが重要です。
なので塩酸でなく水酸化ナトリウムをビュレットやホールピペットに入れて
中和滴定をするのなら、あらかじめ水酸化ナトリウムでビュレットやホールピペットを
すすいでおくということが重要です。
そしてすすいで濡れたままビュレットやホールピペットを使うということが重要です。
中和滴定の器具でもビュレットやホールピペットやコニカルビーカーをを濡れたまま利用する理由
中に入れる溶液でホールピペットやビュレットをすすぎます。
そして乾燥させず濡れたままホールピペットやビュレットを実験に使用します。
乾燥させたらダメです。
それからコニカルビーカーは水ですすいでおいて
やはり濡れたままびしょびしょのまま使います。
で、ビュレット、ホールピペット、コニカルビーカーの基本的な理念は何でしょう?
mol数を一定に保つということが目的です。
酸($H^{+} $)のモル数と
塩基($OH^{ー} $)のモル数がちょうど等しい状態が中和です。
ということなので酸のモル数と塩基のモル数のぶつかり合いなのです。
逆にいうとモル数が狂ってしまうとダメです。
・ビュレットとホールピペットは中に入れる溶液ですすぎ濡れたまま使用
・コニカルビーカーは水ですすいで濡れたまま使用
・上記はモル数を一定に保つため
ということです。

もしホールピペットを水ですすいだらどうなるでしょう?
まずいですね。
どうしてでしょう?
ホールピペットを水ですすいだ後、塩酸を吸ったら
塩酸の濃度が薄くなってしまいますね。
水と塩酸が混ざるから塩酸の濃度は薄くなるのは当然のことですね。
ホールピペットは体積は正確ですからね。
なので水と塩酸が混ざった分、塩酸の濃度が薄くなってしまうわけですよ。
結果、モル数が減ってしまうからモル数が狂ってしまうわけですね。
ビュレットも同様です。
ビュレットも最後に使った体積を正確に測定します。
だから水ですすいでしまうと、中に入れる容積と混ざって薄くなってしまいます。
なので中に入れる溶液ですすいで、中に溶液が入った時に
濃度がわからないようにしないといけないということです。
このように考えるとどうしてビュレットやホールピペットは中に入れる溶液ですすぐのか?
よくわかっていただけたと思います。
逆にコニカルビーカーは入れ物です。
外から正確なモル数を入れるわけです。
だからもし溶液ですすいでしまうと
中に細かいモル数が存在してしまうことになります。
となると周りのモル数が加わってしまうわけです。
なので、外からホールピペットで正確にモル数をとってきてコニカルビーカーに入れて中和滴定します。
もしコニカルビーカーにあらかじめ溶液ですすいでしまうと
細かいモル数が入ってしまい、くるってしまいますよね。
なので余計なものを入れないようにコニカルビーカーは水ですすぎます。
またどうして濡らしておくか?というと
コニカルビーカーの壁面に溶液がこびりついてしまうことがあります。
そうならないようにスムーズに溶液を下まで流すために
コニカルビーカーは水で濡れたまま実験に使用します。
またビュレットやホールピペットが濡れたまま使用する理由は
水酸化ナトリウムなど、乾いてしまうと固体が出ます。
だから濡れたまま使用するわけですね。
本質的なことをいうと『モル数を一定に保つため』
に以上のようなややこしい準備をしているのです。
中和滴定の器具でもメスフラスコの準備の仕方
メスフラスコは純粋ですすぎます。
メスフラスコは乾かす必要があります。
どうしてメスフラスコは乾かすのでしょう?

メスフラスコはピッタリの体積の溶液を作る、つまり薄める器具です。
で、メスフラスコでピッタリ500mLに薄めたとしましょう。
もし水で濡れたまま実験に使用したとします。
すると、細かい水滴がメスフラスコの上部壁面(標線よりも上部分)に残ってしまいます。
標線ギリギリ(500mL)に液体を薄めた後、
このメスフラスコの上部壁面に残った水滴がポタポタとしたたり落ちたら
標線を超えてしまうことになりかねません。
なのでメスフラスコの場合は濡らしておくとまずいです。
だから特に標線より上の部分は乾かしておかないと
ピッタリの溶液を作ったのに、標線より上に存在する水が
ポタポタ落ちて、500mLを超える溶液ができてしまう可能性が生じます。
そうなったら誤差が生じてしまいますね。
そうならないためにメスフラスコの場合、
水ですすいだあと、乾かしてから実験に利用することになります。
・ビュレットとホールピペットは中に入れる溶液ですすぎ濡れたまま使用
・コニカルビーカーは水ですすぎ濡れたまま使用
・メスフラスコは水ですすぎ乾かしてから使用
ということです。
以上、参考にしていただけますとうれしいです。
続いて中和滴定に使用する指示薬の選び方について解説します。