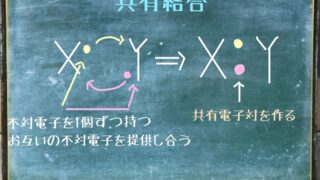今回の記事では極性分子とは何か、
無極性分子と比較しながら簡単にわかりやすく解説します。
極性分子とは?無極性分子と比較しながら簡単にわかりやすく解説
極性とはどういう意味でしょう?
漢字から類推できるかもしれませんね。
極性とは電気の偏りのことです。
つまり、電気陰性度の大きい方に電子が引き寄せられてマイナスに偏り、
電気陰性度の小さい方は電子を持っていかれるからプラスに偏ります。
電気陰性度についてはこちらで解説しています。
⇒電気陰性度とは?わかりやすく解説
ということで極性分子とは電気の偏りを持った分子のことです。
⇒組成式・分子式・示性式の違いについてわかりやすく解説

例えば二酸化炭素分子というのは直線形です(上記画像の右側参照)。
酸素はマイナスに偏って炭素はプラスに偏ります。
「ということは二酸化炭素分子は極性分子ですか?」
と思った方もいるかもしれませんね。
でも違います。
二酸化炭素分子は極性分子ではありません。
無極性分子です。
「でも二酸化炭素分子って両側に酸素のマイナスがあって
炭素のプラスが両側の酸素のマイナスに引き寄せられるから
偏っているんじゃないの?」
って思ったかもしれませんね。
そういうことではありません。
二酸化炭素分子全体としては釣り合っていますね。
二酸化炭素分子は直線になっていて
ちょうどバランスが取れているわけです。
全体として釣り合ったら無極性分子になります。
極性は電気の偏りだってことは定義から明らかです。
でも極性分子というためには分子の形がわからないとダメです。
二酸化炭素というのは均等に偏っています。
だから全体として釣り合っているので無極性分子になります。
ではどういうのが全体として偏っているのでしょう?

水分子(上記画像の左側参照)を考えてみましょう。
水分子は酸素がマイナス、水素がプラスに偏ります。
水分子は折れ線型の形をしています。
だから全体として上がマイナスで下がプラスに偏っているわけです。
これが極性分子です。
こんな感じで極性分子か無極性分子かは
形がわからないと判断ができません。
極性が電気陰性度の差によって起こる電荷の偏りだと覚えているだけでは
極性分子か無極性分子かは判断ができません。
必ず形を覚えるようにしましょう。
極性分子と無極性分子の具体例
・水
・フッ化水素
・塩化水素
・m-ジクロロベンゼン
・アンモニア
です。
・二酸化炭素
・水素
・p-ジクロロベンゼン
・ヘキサン
・メタン
です。
極性分子とは?簡単に解説まとめ
極性分子とは電気陰性度の違いからできる偏りのことです。
⇒電気陰性度とは?わかりやすく解説
これが2原子であればわかりやすいのですが、
3つ以上の原子から分子ができている場合には
極性があったとしても分子の構造が二酸化炭素みたいに対称的な形なら
電気的にバランスが取れてしまい無極性分子になってしまいます。
でも、水分子みたいに直線でない構造をしているなら
上と下で電気的に偏りができ、極性分子になります。
ちなみに塩化ナトリウムは極性分子なのですが、
同じ極性分子である水に溶けやすいです。
つまり、極性分子の溶質は極性分子の溶媒に溶けやすいです。
逆にヘキサンは無極性分子ですが、
同じ無極性分子であるベンゼンに溶けやすい。
つまり、無極性分子は無極性分子に溶けやすいです。
・極性分子の溶質は極性分子の溶媒に溶けやすい
・無極性分子の溶質は無極性分子の溶媒に溶けやすい
です。
これは溶質と溶質の性質が似ているもの同士ほど溶けやすいということです。
以上で解説を終わります。