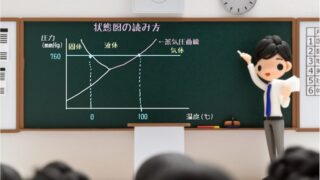
前回の記事では水の状態図を使って
読み方を解説しました。
状態図の見方、読み方が分からない方は先にこちらをご覧ください。
⇒状態図の読み方をわかりやすく解説
今回の記事では二酸化炭素の状態図の特徴を
わかりやすく解説していきたいと思います。
二酸化炭素の状態図について
二酸化炭素の状態図をお見せします。
温度が横軸で、圧力が縦軸です。

それぞれ左から固体、液体、気体になります。
これは前回解説した水の状態図と同じです。
⇒状態図の読み方をわかりやすく解説
以下は水の状態図です。
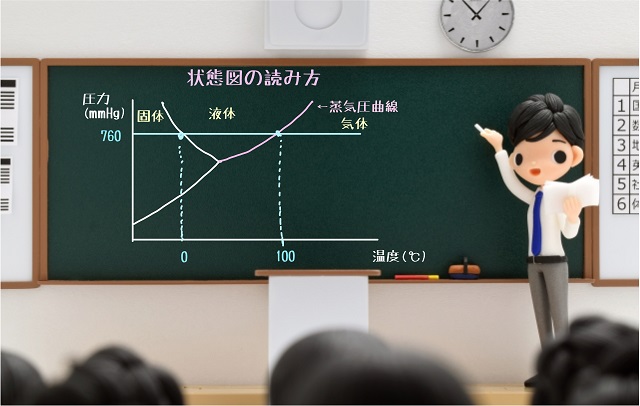
水の状態図と二酸化炭素の状態図を比較すると、
固体から液体に変わるところの曲線が違いますね。

固体から液体に変わるところの二酸化炭素の曲線は右上に向かってます。
でも、水の曲線の方は左上(あるいは右下がりともいえる)に向かっていってますね。
ただ、右下がりの曲線になるのは水くらいといっても過言ではありません。

ほとんどの物質は右上(右上がり)です。
ところで二酸化炭素の固体をドライアイスって言いますね。
直訳すると乾いた氷です。
どうしてそんな名前で読まれるのでしょう?
それは液体にならないからです。
固体から一気に気体が出てくる。
つまり、昇華するからドライアイスって呼ばれるわけです。
ではどうしてドライアイスは昇華するのでしょう?
ちなみに昇華の意味についてはこちらの記事で解説しています。
⇒分子結晶の特徴をわかりやすく解説
二酸化炭素の状態図に大気圧(760mmHg)を書き入れてみましょう。

するとこうなりますね。
地上の気圧は760mmHgです。
上記図をみると、固体か気体しかありません。
温度を下げれば固体になるし、加熱すれば気体になります。
大気圧下では固体か気体しか状態が存在しません。
だから一気に気体になるという昇華性という性質があるわけです。
ここからドライアイスが昇華性を持つ理由が説明できますね。
ではどうして水の氷が一気に水蒸気になる昇華を
見たことないですよね。
どうしてでしょう?
それは大気圧だからです。
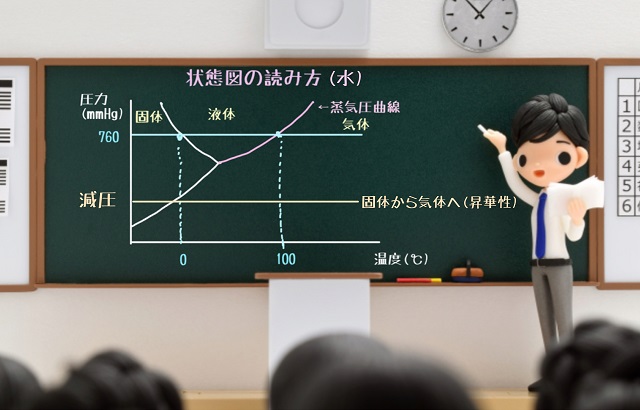
760mmHgという大気圧ではどれだけ温度を上げても
固体⇒液体⇒気体の流れになります。
もし氷を昇華させたかったら減圧するしかありません。
上記状態図のように圧力を下げれば固体から一気に気体になる状態変化が起こるわけです。
水の場合、大気圧下では昇華は起こりません。
でも、ドライアイスは大気圧では液体を通らないところを走っているので昇華性を持つわけです。
こんな感じでいろんな物質の性質が状態図から理解することができます。
固体、液体、気体が温度と圧力で決まるというのを表すのが状態図でした。
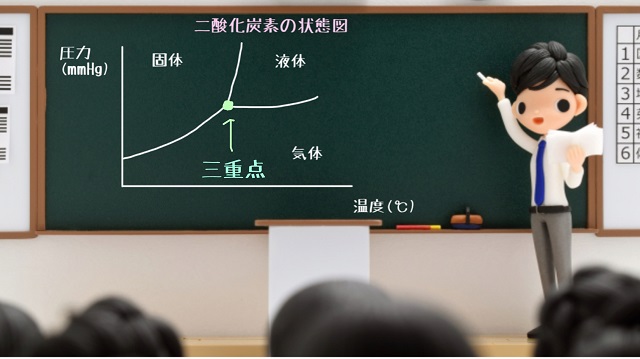
ちなみに3つの曲線が交わるヘソみたいなところを三重点といいます。
三重点というのは、三相間平衡が成立します。
三相間平衡というのは固体、液体、気体という3つの状態が同時に共存できる点です。
こちらの記事で二相間平衡について解説しました。
⇒飽和蒸気圧・気液平衡とは?わかりやすく解説
二相間平衡というのは北極などで存在する液体と固体の共存みたいな話です。
ですが、三重点(さんじゅうてん)という温度と圧力を調節して持ってきた点では、
固体、液体、気体という3つの状態が同時に存在できる変わった状態です。
これが三重点です。
以上で解説を終わります。