今回の記事では分子結晶の特徴について解説します。
分子結晶の特徴
分子結晶の代表選手は二酸化炭素($CO_2 $)です。
二酸化炭素というのは$CO_2 $1分子だけで共有結合ができています。
共有結合について知りたい方はこちらをご覧ください。
⇒共有結合とは?簡単に例を挙げながら解説します
$CO_2 $1分子だけで共有結合ができているということは
別に隣の$CO_2 $とくっつく必要性がないはずです。

こちらの記事で解説した時のC(炭素)なら・・・
⇒共有結合とは?簡単に例を挙げながら解説します
どんどん共有結合できるから
C同士、どんどんくっついても(共有結合しても)問題ありません。
ですが、
こちらの方は$CO_2 $同士でくっつく理由がどこにもありません。
なのに、くっつくことができるのです。
そのときの弱弱しい力のことをなんというのでしょう?
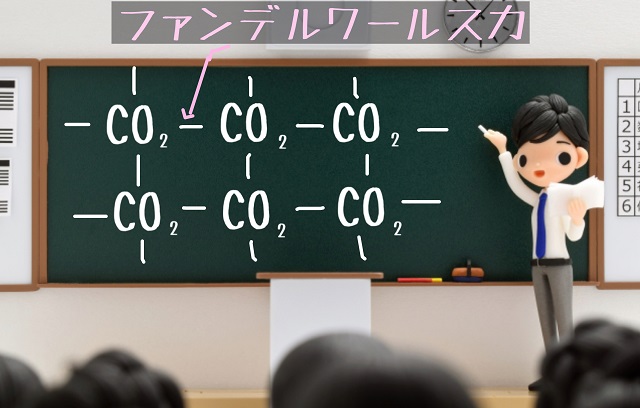
この弱弱しい力のことを『ファンデルワールス力』といいます。
このような弱弱しい力(ファンデルワールス力)でくっついている結合のことを分子結晶といいます。
弱い力でくっついているということは融点とか沸点は非常に低くなります。
結合の強い弱いでどうして融点、沸点が影響するのかについてはこちらの記事で詳しく解説しています。
⇒共有結合結晶とは?わかりやすく解説
それから
・ドライアイス(二酸化炭素が固体になったもの)
・ナフタレン
・ヨウ素
などを挙げることができます。
このファンデルワールス力ですが、
ものすごく結合力が小さいです。
結合力が強ければ火であぶられても離れませんが、
分子結晶は結合力が弱いので、少し火であぶられるだけで離れてしまいます。
どれくらい弱いのでしょう?
こちらの図をご覧ください。
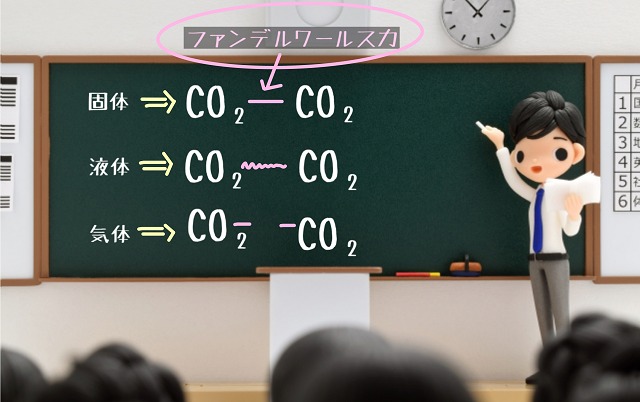
図の一番上を見てください。
$CO_2 $同士でファンデルワールス力があったとしてください。
しっかりと結合している状態なので固体です。
固体の下の結合はファンデルワールス力が弱くなった状態が液体の状態です。
さらに下、ファンデルワールス力が切れた状態が気体です。
普通は上記のように(氷を想像してください)、
固体から液体、気体に変化します。
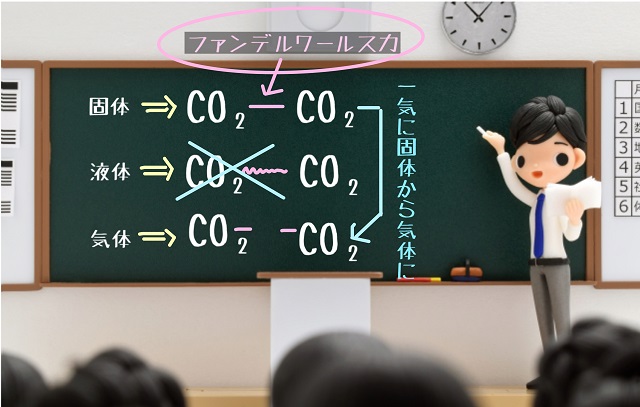
ですが、ファンデルワールス力は液体を経由しません。
弱い結合だからです。
固体から一気に気体に行ってしまうのです。
ちょっと中途半端な液体の状態を一気に飛び越して気体の状態になってしまいます。
このように固体からいきなり気体に行く性質のことを昇華性(しょうかせい)といいます。
昇華性は固体から気体、気体から固体といった感じで
液体を介さない現象のことをいいます。

たとえばドライアイスは昇華性をもっています。
あなたはドライアイスというと何を想像しますか?
保冷剤と答える方が多いはずです。
私がこの記事を書いているのは2021年8月22日です。
めちゃくちゃ暑いです。
アイスクリームが食べたいです。
もしお店でアイスクリームを買って
自宅に持ち帰ろうとしたら、
ちょっと洒落たお店なら「お持ち帰りのお時間はどれくらいですか?」
と聞かれるでしょう。
すると、ドライアイス入りの入れ物にアイスクリームを入れてくれるはずです。
これ、保冷剤としてドライアイスを使っているからよいわけです。
たとえば物を冷やすだけなら氷でもOKでしょう。
でも、氷入りのアイスを自宅に持って帰ってきたときには
氷が解けてびしゃびしゃになっていることでしょう。
でもドライアイスは昇華性があって、
液体にならないで気体になるので、びちゃびちゃになりません。
だからドライアイスが保冷剤としてよく利用されているわけですね。
以上で分子結晶についての解説を終わります。