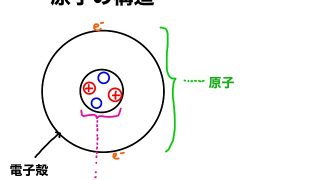
前回の記事では気液平衡や飽和蒸気圧について解説しました。
⇒飽和蒸気圧・気液平衡とは?わかりやすく解説
ここまでの内容を読んでいただけたらわかっていただけると思いますが、
物質を決めるための要素って温度だけではありませんね。
圧力によっても物質の状態は変わってきます。
飽和蒸気圧になったら蒸発せずに液体が残るわけですからね。
⇒飽和蒸気圧・気液平衡とは?わかりやすく解説
温度だけで全部気体になったり液体になったり固体になったりするとはいえません。
・温度
・圧力
の2つが関係していることがわかります。
温度と圧力という2つの要素によって物質の状態が決まります。
これを表す図が状態図です。
今回の記事では状態図の読み方についてわかりやすく解説していきます。
状態図の読み方
物質の状態は温度だけでなく圧力によっても変わってきます。
このことを表す図を状態図といいます。
今回の記事では水の状態図を使って説明していきますね。
まず横軸と縦軸をとって座標平面図を書きましょう。
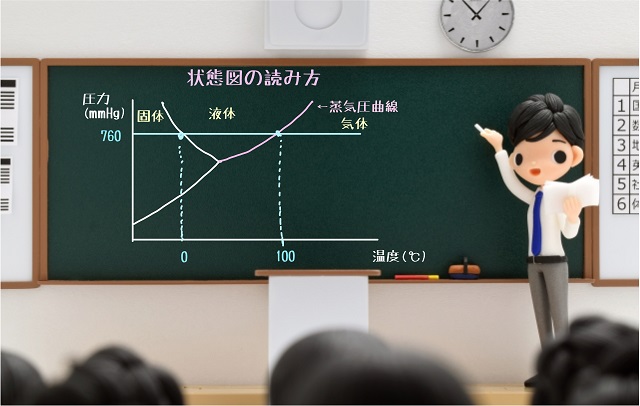
横軸に温度(℃)、縦軸に圧力(mmHg)とします。
mmHgは『ミリメートル水銀』と読みます。
⇒mmhgとは?意味を図を使ってわかりやすく解説
この座標平面に3つの曲線を書き入れて、3つの領域に分けています。
それぞれの領域がある物質(ここでは水)のその状態を表しています。
温度と圧力が決まれば1つに状態が決まるようにできた図が状態図です。
まずはどの領域が何体を表現しているのか特定していきましょう。
ここでは水について考えています。
普段、生活している1気圧という世界で考えてみるのが一番わかりやすいでしょう。

1気圧というのは760mmHg(大気圧)です。
760mmHgのラインを上記図のように横線でまっすぐ引っ張っていきましょう。
1気圧という圧力のもと、温度を上げていきましょう。
0℃のところで固体から液体に状態変化しています。
100℃のところで液体から気体に状態変化しています。

だから左端が固体の領域、真ん中が液体の領域、右端が気体の領域だとわかりますね。
ちなみに蒸気圧曲線というのはピンク色の線のことを指しています。
大気圧下(1気圧、760mmHg)では100℃で沸騰します。
100℃で蒸気圧が大気圧と同じ760mmHgに達するから100℃で沸騰するといえます。
沸騰についてはこちらの記事で詳しく解説しています。
⇒蒸発と沸騰の違いについてわかりやすく解説
とにかく温度と圧力で状態が決まるということを言っているのが状態図です。
では気圧が1気圧より低い状況を考えてみましょう。
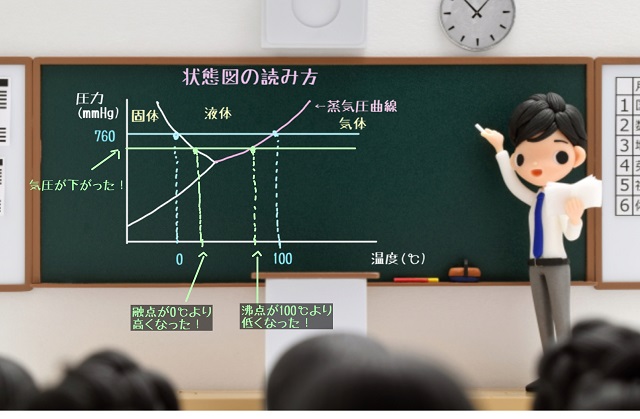
気圧が低くなると固体から液体に変わる融点は0℃より高くなりますね。
逆に沸点は100℃より低くなりますね。

たとえば、富士山の山頂。
富士山の山頂は気圧が低いし空気は薄いです。
すると沸点は100℃よりも低くなります。
より低い温度で沸騰する事が可能になります。
ということが状態図からいえますね。
上からのしかかっている圧力が小さいなら
より低い温度で沸騰できるということが状態図からわかりますね。
逆に圧力を高めたら(加圧したら)どうなりますか?
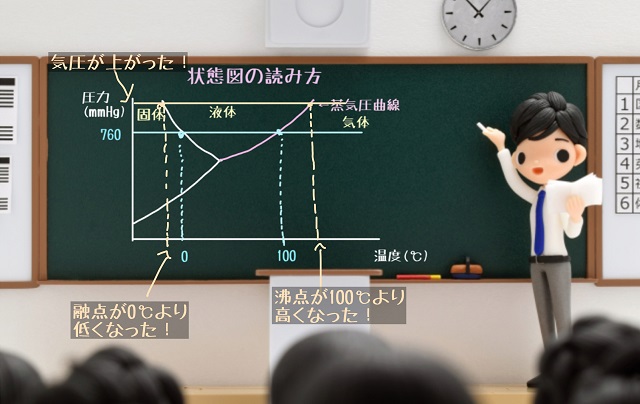
固体が液体に変わる温度は0℃より低くなり、
液体が気体になる温度は100℃より高くなりますね。
圧力が高くなると、水の沸点は100℃より高いところになりますね。

これを利用したものが圧力鍋です。
圧力鍋の中はだいたい2気圧くらいまで加圧ができます。
すると水の沸点は180℃くらいまで高まります。
沸点が上がるということは100℃より高温に加熱してもまだ水は沸騰しませんね。
水を沸騰させることなく、100℃以上の温度まで加熱ができます。
結果的に、調理時間が大幅に短縮できるわけです。
圧力鍋の原理です。
加圧する事で沸点を高めるとどんなメリットがあるのでしょう?
水を沸騰させることはないということは具は焦げません。
具が焦げずにより高温まで加熱できるので短時間で火が通って
調理が完了します。
調理時間の短縮を図ることができる鍋を圧力鍋といいます。
こんなことも状態図からわかります。
状態図はいろんなことがわかりますね。
以上で状態図の読み方についての解説を終わります。