前回の記事では電子式を使って共有結合を一緒に作ってみましたね。
「まだやってないよ!」という方は
先にこちらの記事を読んでみてくださいね。
でないと今回の構造式がまったくチンプンカンプンになってしまいますからね。
⇒共有結合とは?簡単に例を挙げながら解説します
⇒電子式書き方の決まりをわかりやすく解説
化学で取り扱う構造式とは共有電子対を一本の線分で表現したものです。
以下例を挙げて構造式を作っていきます。
構造式とは?具体例を挙げながら一緒に作っていこう!
こちらは前回の記事でやった水の電子式です。
⇒共有結合とは?簡単に例を挙げながら解説します
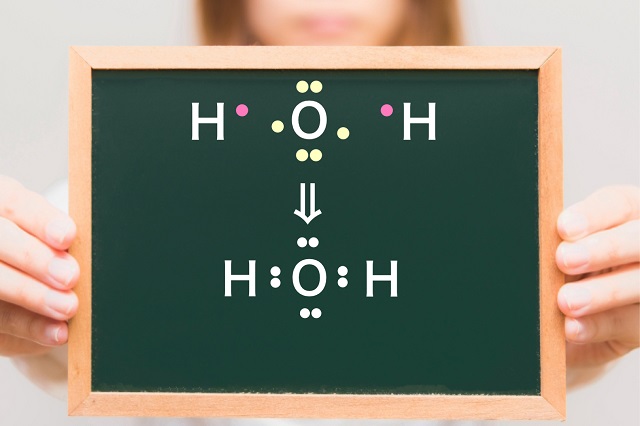
水分子は共有電子対が両サイドについていますね。
これを一本の線分で表現したものが構造式です。

だから、水分子の構造式は電子式が簡略化された形になります。
黒ぽちをいっぱい使わないといけない電子式と比べると構造式は非常にシンプルです。
構造式は非共有電子対(酸素Oの上についている二個の●●のこと)は無視してください。
書かなくてよいです。
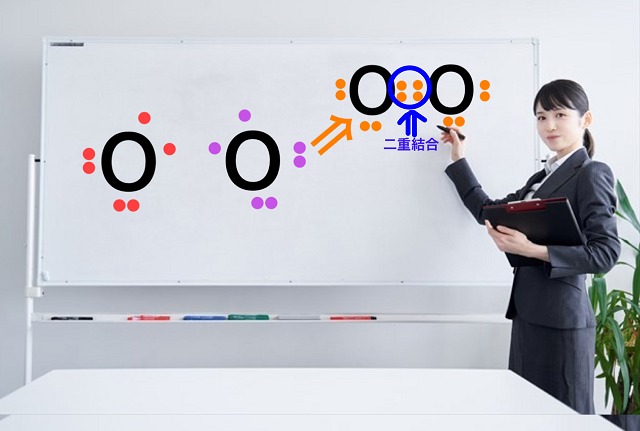
では$O_2 $(酸素分子)の構造式はどうなるでしょう?

$O_2 $(酸素分子)は二重結合でしたね。
なので、こちらのように構造式は二重線で表します。
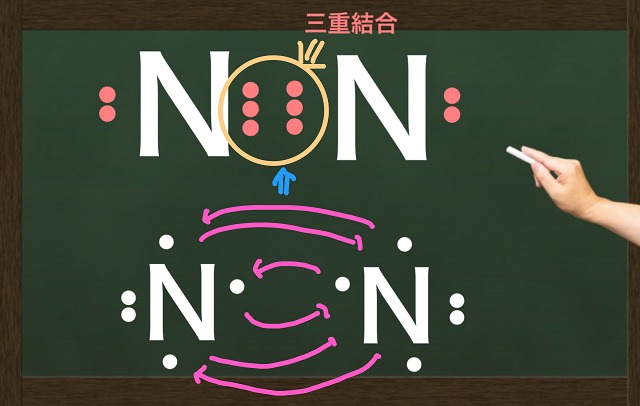
では$N_2 $(窒素分子)はどうでしょう?
窒素分子は三重結合でしたね。

酸素分子は二重結合で二本線でしたから
同様に三重結合は三本線で表します。
構造式とは共有電子対を線分で表現したものになります。

構造式で使う線分ですが、価標(かひょう)といいます。
つまり、価標という線分で共有電子対を表現したものが構造式になります。
以上で構造式についての解説を終わります。















