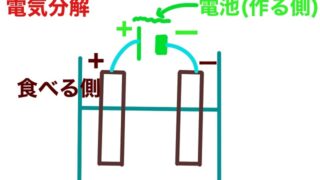
前回イオン結合について解説しました。
⇒イオン結合とは?簡単にわかりやすく解説
今回の記事ではイオン結合からできるイオン結晶の特徴についてわかりやすく解説します。
ただ、先にイオン結合の復習をしておきたいと思います。
Contents
イオン結合とは?
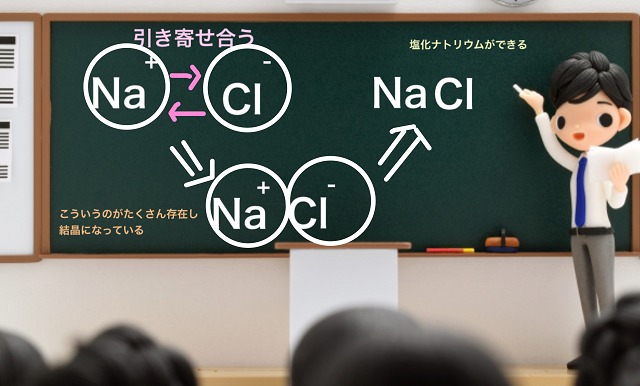
$Na^+ $(ナトリウムイオン)と$Cl^- $(塩化物イオン)を例に
考えていきましょう。

まずプラスのものとマイナスのものってどんな力が働くでしょう?
磁石のN極とS極は引き合う力が働きますね。
でもN極同士、S極同士だったら反発する力が働きます。
電荷も同じです。
プラス同士、マイナス同士は反発するけど、
プラスとマイナスという異符号同士だったら引き合う、引力が働きます。

なので陽イオンである$Na^+ $(ナトリウムイオン)と陰イオンである$Cl^- $(塩化物イオン)
は互いに引き合う力が働きます。
このとき引き合おうとする力のことをクーロン力といいます。
クーロン力は静電気力ともいいます。
とにかくクーロン力(静電気力)によって陽イオンと陰イオンがくっつくわけです。
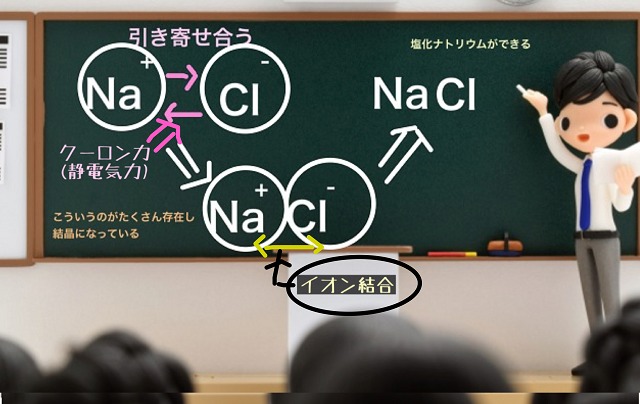
陽イオンと陰イオンがくっつくことで結びつきができるわけです。
この結びつきのことをイオン結合といいます。
こんな感じで陽イオンと陰イオンがくっついた状況を記載しましたが、
クーロン力という引力にしたがって他にもイオンがいっぱいくっついてきます。
$Na^+ $(ナトリウムイオン)の空いたスペースに対しては$Cl^- $(塩化物イオン)が、
$Cl^- $(塩化物イオン)の空いたスペースには$Na^+ $(ナトリウムイオン)がくっついてきます。

最終的にはたくさんの陽イオンと陰イオンが交互にならんだ集合体になります。
書ききれないくらいたくさん集合し固体が出来上がります。
これをイオン結晶といいます。
別に$Na^+ $(ナトリウムイオン)と$Cl^- $(塩化物イオン)の組み合わせでなくても構いません。
他の陽イオンと陰イオンの組み合わせでもOKです。
ではこのイオン結晶ってどんな特徴があるのでしょう?
イオン結晶の特徴

上記画像は塩化ナトリウムの固体です。
塩化ナトリウムって食塩ですね。

食塩ってどんな形をしていますか?
砂みたいですね。粉砕された状態です。

ただ岩塩というのはもともとは大きな固体(塊)です。
でも私たちが使う食塩は粉々に砂みたいになってますね。
イオン結晶は簡単にボロボロと壊れていきます。
粉砕してしまいます。
どうしてでしょう?
クーロン力によりイオン結合というのは弱い結合ではありません。
イオン結合は共有結合の次に強い結合です。
ではどうしてそんな簡単に壊れてしまうのでしょう?
それはこちらの形を見ると理解できます。

陽イオンと陰イオンが交互に規則正しく並んでいますね。

もし力を加えて(衝撃を与えて)下側の配列を1つ右にずらしたらどうなるでしょう?
すると、$Na^+ $(ナトリウムイオン)の下に$Na^+ $(ナトリウムイオン)が、
$Cl^- $(塩化物イオン)の下に$Cl^- $(塩化物イオン)がきますね。
1つ配列がずれると同じ符号のイオンが向かい合うことになります。

するともちろん反発し合いますね。
プラス同士、マイナス同士で。
そこからボロボロと壊れてしまうわけです。
ですから配列がずれなければイオン結合という強い結合なので硬いです。
でもちょっと力を加えると(衝撃を与えると)ボロボロ削れてしまうという特徴があります。
・硬いけどもろい
があります。
イオン結晶の特徴は他にもあります。
まずイオン結晶は固体の状態では電気は導きません。
プラスとかマイナスという電気を持った粒が動くことによって電気が通ります。
つまりプラスやマイナスの電気が動かないと電気は通らないということです。
イオン結晶というのはプラスやマイナスのイオンが動けません。
クーロン力で完全に固定されているから自由に動ける状態ではありません。
つまり、固体というのは電気を持った粒が動けない状態のため電気を通しません。
でも、液体だと陽イオンと陰イオンの結びつきが緩くなって動きます。
自由にマイナスやプラスのイオンが動けるようになるので
電気を通すようになります。これを電気伝導性があるといいます。
・固体の状態だと電気は通らない
・でも液体、水溶液は電気を通す
ということです。
たとえば、家にある食塩に電極を差し込んでも電気は流れません。
食塩は固体だからです。
でも、食塩『水』にして電気を通したら電気は流れます。
イオン結晶の特徴は
・硬いけどもろい
・固体の状態だと電気を通さない
・でも液体になると電気を通す
ということです。
続いてイオン結合より結合力の弱い金属結合について解説します。
⇒金属結合とは?例を挙げながらわかりやすく解説