今回の記事では活性化状態(活性化エネルギー)とは何なのか、
分かりやすく解説していきたいと思います。
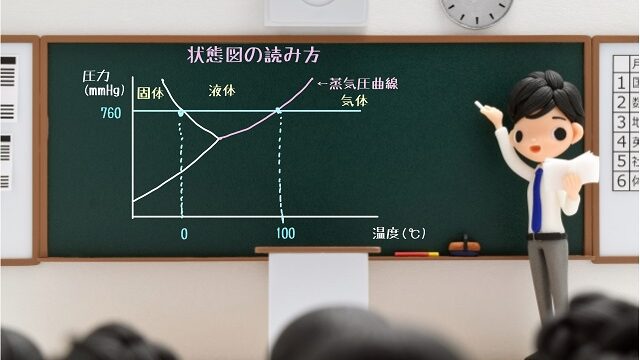
活性化エネルギー(活性化状態)とは?
活性化状態について説明するために架空の物質を例に解説していきますね。
今、以下のような化学反応が起きたとしましょう。
$X_2 $+$Y_2 $⇒$2XY $+$Q KJ $($Q>0 $)
今回はQ(KJ)発熱すると考えます。
Q>0より発熱です。
発熱反応というのはエネルギーの高い状態から
より低い状態に変化した時に起こる反応です。
高いエネルギーと低いエネルギーの差が発熱反応となります。
⇒発熱反応で温度が上昇する理由とは?
⇒発熱反応が発生する身近な例
⇒熱化学方程式とエネルギー図で発熱と吸熱反応を表すコツ
なので、エネルギーの関係を表すエネルギー図を書いてみますと、、、
⇒熱化学方程式とエネルギー図で発熱と吸熱反応を表すコツ
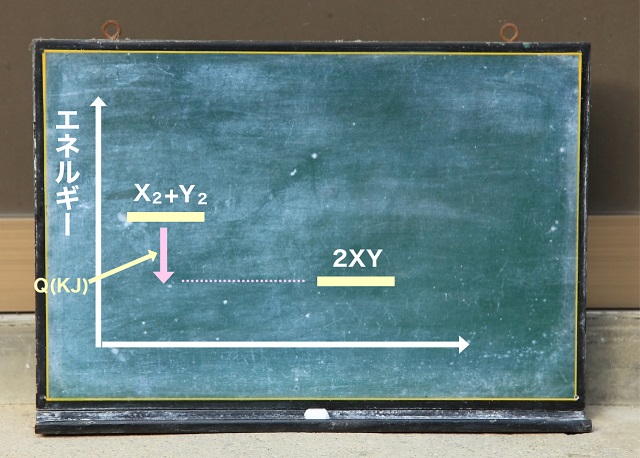
X2、Y2というスタートの状態と、2XYという生成物の状態を比較したら
この生成物の状態(2XY)の方がQ(KJ)だけ低くなります。
エネルギーの高いところから低い所に変化したら外に熱が放出され
発熱反応が起こるわけですね。
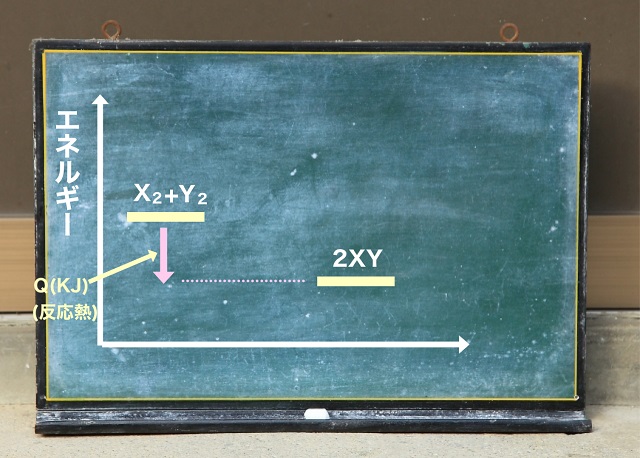
このQ(KJ)のことを反応熱といいます。
発熱反応というのはエネルギーの低いところに変化が起こるわけです。
吸熱反応だったら逆でゴール地点の方が高くなります。
⇒熱化学方程式とエネルギー図で発熱と吸熱反応を表すコツ
エネルギーって高い時と低い時、どちらの方が安定していると思います?
物質が持つエネルギーは高いほど不安定で低いほど安定します。

物が高いところから低い所に勝手に落ちるように
エネルギーもより低いところに向かおうとして反応は進んでいきます。

エネルギーは高いほうが不安定で、
低くなればなるほどエネルギー的には安定であるといえます。
なので発熱反応というのはエネルギー的により安定な方向に向かう反応だと
言えるわけですね。
ということは発熱反応ってこちらから
何もしなくても勝手に起きてもよさそうですよね。
エネルギーに安定な方向に反応が進むわけだから
特に何かしなくても勝手にどんどん連鎖的に反応が進んでもよさそうです。
でも、どうですか?
発熱反応であっても最初、何かしらのきっかけを与えてから
反応が起こり始めてませんか?
こんな経験ありませんか?

たとえばホッカイロって鉄粉が酸化されるときに発熱することを利用していますが
カイロをあっためるときって、こすったり振ったりすることで摩擦熱を与えてますね。
買った瞬間から熱くなっているものがあったら、買いませんよね。
買った瞬間は熱くないけど、袋を開けて振ったりこすったりすると
じわじわ熱が出ますよね。
発熱反応が開始するってことです。

あるいはマッチで火をつけるときどうします?
⇒マッチ棒を擦るとどうして火がつくの?化学的にわかりやすく解説
マッチ棒を持っているだけでは火はつきませんよね。
マッチ箱の横の赤リンの部分とこすり合わせることで火が出ます。
持っていて火が出たらマジックです。
こすって摩擦熱を与えることで火が出るわけです。
擦らないと火が出ません。
ライターで火をつけるときも同様です。
ライターだってダイヤルみたいなのを回すことでガスが出て火が出ます。
こすったときに火花が飛んで、この火花にガスが引火して火になります。
今、3つ例を挙げましたが、全部発熱反応の身近な例です。
でも発熱反応ですが、なにかしら外部からきっかけとなるエネルギーを与えてから
反応が始まってますね。
こすったり火花飛ばしたりと。
発熱反応でも勝手には反応は開始しませんね。
きっかけとなるエネルギーを外部から与えています。
どうしてでしょう?
エネルギーなんて与える必要なさそうですが。。。
エネルギー的に安定な方向に向かうわけですし。
どうして外部からエネルギーをあたえないといけないのでしょう?
実は反応前と反応後の間にたとえ、発熱反応であっても
一時的にエネルギーの高い状態が存在するのです。
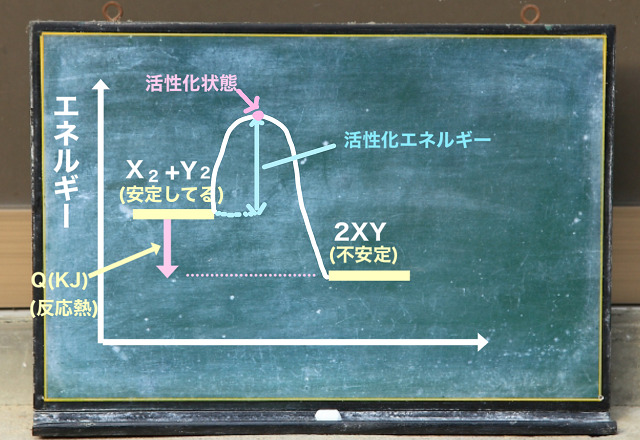
上記図のようにエネルギーが高い状態を経由しないと反応って進行しないのです。
このエネルギーの高い山を越えるためのエネルギーを与えているのが
カイロをこすったり、ライターで火花を飛ばしたりという行為です。
この最もエネルギーの高い状態を『活性化状態』といいます。
活性化状態というのはすごく不安定な状態ですが、
この活性化状態を経由して反応が起こるのです。

で、スタートから山のてっぺん(活性化状態)になるまでに必要となるエネルギーのこと、
山の高さですが、これを活性化エネルギーといいます。
活性化状態になるまでのエネルギー(活性化エネルギー)を外部から
最初に与えてあげないと反応が開始しないわけですね。
これが反応が起こる仕組みです。
一時的にエネルギーが高い状態を通らないと反応が起こらないことを
知っておきましょう。

最初反応さえ起きてしまえば、次の反応の活性化エネルギーは
この反応熱を使って山を越えることができます。
だからホッカイロをこするのも最初だけでOKです。
あなたはずっと朝から晩までホッカイロをこすってませんよね。
最初だけホッカイロを擦って暖かくなったら
ポケットに入れるなどして放置してますよね。
それは最初さえ活性化状態にまでもっていけば
あとは反応熱のエネルギーで反応が続いていってくれるからです。
この活性化状態ってどんな状態でしょう?
もともとあった古い結合が切れつつあり
代わりにXY間に新しい結合ができつつあるような
そんな結合の組み換えが同時に起きている状態です。
一言でいったら活性化状態は結合の入れ替えが同時進行で起きている状態と
理解しておけばよいでしょう。
ところで反応の速さって何で決まるのでしょう?
次回は反応速度について解説します。