今回の記事では
イオン化傾向と水との反応で覚えるべきポイントについて
わかりやすく解説していきます。
イオン化傾向と水との反応
イオン化傾向と水との反応で覚えるべきポイントを
ご紹介していきますが、先にイオン化傾向を暗記しましょう。
下ネタバージョンとかジャニーズバージョンなどがあるので
あなたが覚えやすい語呂合わせで覚えてください。
前回の記事で解説しましたが
イオン化傾向というのは還元剤の強さを表すもののことでしたね。
こちらの記事で解説しています。
⇒イオン化傾向の覚え方(ジャニーズや下ネタを活用)
還元剤についてはこちらで解説しています。
⇒酸化剤と還元剤語呂を使った覚え方
話を元に戻しますね。
K>Ca>Na>Mg>Al>Zn(亜鉛)>Fe(鉄)>Ni>Sn(スズ)>Pb(鉛)>(H2)>Cu>Hg>Ag>Pt>Au
貸そうかなまああてにすんなひどすぎる借金
K(貸そう)>Ca(か)>Na(な)
>Mg(ま>Al(あ)>Zn(あ)>Fe(鉄)>Ni(に)>Sn(すん)>Pb(な)
>(H2)(ひ)>Cu(ど)>Hg(す)>Ag(ぎる)>Pt(借))>Au(金)
です。
イオン化傾向が大きいほど
『還元剤として強い=水と反応しやすい』。
反応性が高いということです。
では本当に反応性が高いかどうかチェックするために
水と反応させてみましょう。

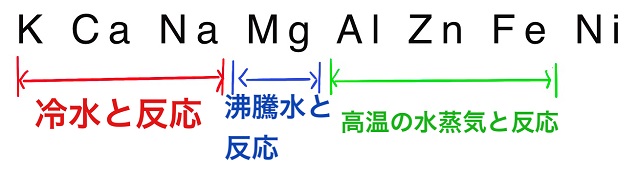
カリウム(K)やカルシウム(Ca)やナトリウム(Na)を
冷たい水の中に入れるといきなり反応します。

ですが、Mg(マグネシウム)になると
冷たい水をかけてもほとんど反応しません。
そこで加熱して沸騰させます。
すると反応します。
こんな感じでイオン化傾向が右に行けば行くほど
だんだん反応性が低くなります。
Mg(マグネシウム)は沸騰水と反応します。
それからAl(アルミニウム)、Zn(亜鉛)、Fe(鉄)についてですが。
アルミの鍋でお湯を沸かしても別に反応しませんね。
反応したら困ってしまいます。
海水からの塩作り、自宅に帰り火にかけて2時間弱で固体化してきた
家のお鍋はアルミニウム鍋だけど厚さが厚いので錆が出たり、ボコッボコッと沸騰しない、これから自宅で作るかな…
あっという間に塩が析出してきた、あともう一息 pic.twitter.com/PUAZCmvgBd
— ekoro (@ekoro15) December 18, 2022
どんどん加熱して水蒸気にしたとしましょう。
私たちはイメージとして水蒸気=100℃くらいを
イメージすると思います。
ですがあなたが生活している部屋が
500℃になったとしましょう。あり得ないですけど。
部屋が500℃になれば、部屋の中には水蒸気があるので
500℃の水蒸気を作れます。
なのでものすごい高温の水蒸気を作ることは可能です。
ここで言っているのは200℃、300℃の高温の水蒸気です。
そんな高温の水蒸気とAl(アルミニウム)、Zn(亜鉛)、Fe(鉄)は
反応します。
だから水蒸気でマッチに火をつけることもできます。
温度の高い水蒸気をマッチにぶつければ火がつきます。
土曜日はサイエンスショー
2月のテーマは【燃焼の実験】
燃えるための条件は
1⃣燃える物であること
2⃣酸素があること
3⃣温度が高いこと温度を上げてあげれば、水(水蒸気)でもマッチに火を点けることができます🔥
毎週土曜日 13:30~、15:30~#サイパル #実験 #燃焼 #科学館 pic.twitter.com/bQdfZfHU4O
— 旭川市科学館 サイパル (@scipalAsahikawa) February 10, 2022
で、イオン化傾向がFe(鉄)よりも小さくなると
いくら水の温度を上げても反応しません。
イオン化傾向が左にあるものほど(大きいほど)、
水との反応性が高いということです。
ナトリウム(Na)と水との反応(イオン化傾向)
たとえばNa(ナトリウム)を水に溶かしたとしましょう。
するとNaと$H_2O $のHが置き換わって
NaOHと水素ガスになります。
式で表すと以下のようになります。
2Na+2$H_2O $⇒2NaOH+$H_2 $
となります。
こんな感じでナトリウムと水を反応させると
水酸化ナトリウムと水素になります。
しかもこのとき、かなりの熱が出ます。
かなり熱が出るので
この熱が水素に引火して爆発します。
だから大変危険です。
ビーカーに水を入れてナトリウムの塊を入れたら
爆発するので絶対にやったらダメです。
ナトリウムは水に触れると爆発するから
危ないんだよ!(● ˃̶͈̀ロ˂̶͈́)੭ु⁾⁾ちなみに反応式は
2Na + 2H₂O → 2NaOH + H₂ な! https://t.co/sFDK2lsrzp pic.twitter.com/msQ436CMRX— 境 宏樹 ⌬ FRACTAL[ 理系バー ] (@Piron_glba) January 22, 2023
なのでナトリウムを細かく刻んで
ほんの小さな点くらいのナトリウムの粒を
水の入ったビーカーに入れます。
するとナトリウムが水と反応して水酸化ナトリウムになりながら水素ガスがでます。
また、ナトリウムは水より密度が小さいので浮きます。
ということでこの水素ガスに引火して
火を出しながら小さいなとリムが水の上を走り回ります。
ナトリウムは水に触れると爆発するから
危ないんだよ!(● ˃̶͈̀ロ˂̶͈́)੭ु⁾⁾ちなみに反応式は
2Na + 2H₂O → 2NaOH + H₂ な! https://t.co/sFDK2lsrzp pic.twitter.com/msQ436CMRX— 境 宏樹 ⌬ FRACTAL[ 理系バー ] (@Piron_glba) January 22, 2023
こういった情報を知っておくと
万が一、ナトリウムを使うようなことがあったときに有益です。
今回の情報を知っていれば、火が出た時に水をかけたら
爆発するということがわかるわけです。
ナトリウムに水をかけるのは危険。
だから実験室には砂が置かれています。
私が所属していた大学時代の研究室にも砂が置かれていました。
⇒当ブログ管理人のプロフィールはこちら
スゲー懐かしい事案がヒットした・・・
どっかの実験室でナトリウムか何かが発火して。
危険物取扱者取得したときのおぼろ気な知識で「水かけずに乾燥した砂かけろ」ってアドバイスした記憶がある。 https://t.co/QMtIGkX18g— 男爵_赤松先任曹長 (@akamachu) October 14, 2016
ナトリウムの実験で火か出たら砂をかけましょう。
水をかけたら余計に火が出ますから。
これは危険物取扱者試験でも頻出のテーマなので
必ず覚えておきましょう。
昔、ナトリウム漏れ事故がありました。
おはようございます。
気温5度、湿度70%
12月8日は「きょうはなんの日」もりだくさんですね。
日本が米英に宣戦布告(1941年)
ジョン・レノン命日(80年)
ソ連の事実上崩壊(93年)
もんじゅナトリウム漏れ事故(95年)トレンドの五条悟先生誕生日(89年)は昨日。。(シマッタ)
— Aya N |内面を深掘りするライター/編集者|上級ウェブ解析士 (@Ayan_unicla) December 7, 2022
ナトリウムというのは扱いが難しい金属だということです。
ちょっとでもナトリウムが大きいと爆発するリスクがあります。
気をつけてください。
あと面白い実験としては
水の入ったビーカーに細かいナトリウムを入れ
反応している時に、フェノールフタレインを入れます。
アルカリ性の溶液にフェノールフタレインを入れると赤色になります。
水にナトリウムを入れるとアルカリ性の水酸化ナトリウムができますね。
だから事前にフェノールフタレインの水溶液を入れておくと
小爆発を起こして走り回る水酸化ナトリウムに
赤色もくっつきながら続いて見えるという姿を見ることができます。
【Naと水の反応】
金属ナトリウムを水に濡らしたろ紙の上に落とすと黄色の炎を上げながら激しく反応するよ!発生した水素に引火し、軽い爆発も…
2Na+2H2O→2NaOH+H2
NaOHより、フェノールフタレインを入れると赤く!pic.twitter.com/mRn9y7kNhP— 実験たん (@Experiment_tan) January 22, 2023
今回の記事ではイオン化傾向と水との反応で覚えておいた方がよい
ポイントについて解説しました。
参考になっているようでしたらうれしいです。
続いてイオン化傾向と酸との関係について解説します。
⇒イオン化傾向|酸との反応についてわかりやすく解説














