今回の記事では
・金属結晶
・イオン結晶
の性質の違いについて解説します。
Contents
イオン結晶と金属結晶の性質の違いとは?
イオン結晶と金属結晶の性質の違い(1)電気伝導性

前回の記事で解説しましたが
金属結晶(金属結合と同じ)は自由電子というものによってくっついた結晶(結合)のことでしたね。
自由電子というくらいですから
電子が自由に動くわけです。

そこに電圧をかけると
自由電子が上記図のように自由に移動し電流が発生します。
電流が発生、つまり電気が流れるってことです。
このことを電気伝導性といって金属結合の性質の1つでもあります。
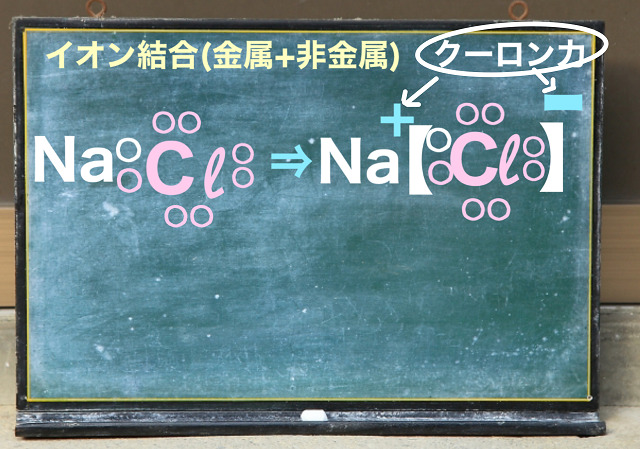
これに対してイオン結晶(イオン結合と同じ)はクーロン力で結合しているのでしたね。
自由電子が自由に動き回る金属結晶とクーロン力は全く違います。
金属結晶の自由電子なら電子が自由に動き回り電気伝導性がありましたが
クーロン力は自由に動けないので電気伝導性はありません。
ここが金属結晶とイオン結晶の性質の違いとなります。
ただし、イオン結晶は水に溶かして水溶液にした場合には
電気伝導性を持つようになります。
イオン結晶と金属結晶の性質の違い(2)硬さやもろさ

まずイオン結晶(イオン結合)ですが、上記図のように規則正しく並んでいる状態で、
ハンマーで横に叩くとしましょう。
すると、

上記図のように配列がずれてしまいます。

結果、プラスとプラス
マイナスとマイナスがぶつかり合い、反発し合います。
磁石を想像するとわかりやすいですが、マイナス同士、プラス同士は反発しあって離れますね。
結合が崩れるってことです。
つまりイオン結晶は結合は強いけど『もろい』という性質があります。

これに対して金属結晶は
もしハンマーで叩くなどの衝撃を受けて配列がずれたとしても
自由電子が自由に動き回ってくれているので
すぐにプラスとマイナスでくっついてくれるのです。
ということで、金属結晶(金属結合)だと電子殻同士が接触していれば
自由電子のおかげで結合が離れることがありません。
だから金属結晶は衝撃によっても壊れたりしません。
だから金属結晶は『もろく』ありません。
・イオン結晶はもろいけど、金属結晶はもろくない
・イオン結晶は電気伝導性はないけど、金属結晶にはある
という違いがあります。
ここでもうちょっと金属結晶について知りたい方のために
復習ということで再度、金属結晶の性質について解説しておきますね。
金属結晶の性質
化学で登場する固体には2種類ある!
これから解説するのは固体です。

・結晶
・無定形固体(むていけいこたい)
の2つがあります。
原子や分子、イオンが規則正しくきれいに並んでいるものを結晶といいます。
ある一定のリズムを持って原子、分子、イオンが貴族正しく並んでいるものを結晶といいます。
つまりリズムパターンが一定の固体を結晶といいます。
規則正しく並んでいる結晶に対して
規則正しく並んでいない固体もあります。
めちゃくちゃ熱くしてドロドロにして液体にして
そこから急激に冷やすと規則正しく並べなかったりします。
こんな感じで貴族正しく並んでいない固体を『無定形固体(むていけいこたい)』といいます。
ということで
・規則正しく張り付いているのを結晶
・ぐちゃぐちゃにくっついているのを無定形固体
といいます。
ただ、高校の化学では固体というと普通は結晶を勉強することになります。
ちなみに
・ゴム
・ガラス
・光ファイバー
・石英ガラス
などがあります。
加熱して急激に冷やしたりすると形が定まらない無定形固体になります。
もちろん、金属固体は金属結晶ともいうので、規則正しく結合しています。
では規則正しい金属結晶の性質について解説していきますね。
金属結晶の性質についてわかりやすく解説
金属が規則正しく並んでいるのが金属結晶です。
これもある意味金属結晶の性質の1つといえるでしょう。
結晶は規則正しく並んだものだという知識があるだけで
性質を1つ言えてしまうのですね。
それから金属結晶は金属結合のことだと
この記事ではひたすら説明していますね。
金属結晶というのは金属結合からできたもののことです。
では金属結晶の性質を理解するためにナトリウムを使っていきますね。

ナトリウムというのは最外殻電子が1個です。
最外殻電子が自由気ままに1個の電子を放り投げてプラス1になりますね。
そして1個の電子が1つのナトリウムイオンの周りをグルグル
周っているわけではなくて全体を自由きままに動き回っています。
そんな自由気ままに動き回っている電子を自由電子といいます。
そんな自由電子のおかげで金属は電気を導いたり熱を伝えたりします。
電気や熱を導くという性質がある

あと自由電子のおかげで金属には独特の光沢があります。
あまり金の延べ棒をジーッと眺めたりはしないでしょうけど、
できれば頭の中で想像していただけると分かりやすいかと思います。
なぜ金属結晶には独特の光沢があるのでしょう?
理由としては自由電子が光を反射することで独特の光沢が出るのです。
つまり、
自由電子が光を反射する結果、独特の光沢がある
また、自由電子が自由気ままに動いてくれるので加工することができます。
金属結晶の中身がちょっとずれてもスーッと自由電子が動いてくれるので
くっつきます。
だからずらしたり、叩いたり、伸ばしたりしても
自由電子がフォローしてくれるので壊れず変形するだけで終わります。
そのおかげで金属結晶は加工しやすいという性質があります。
たとえば銅を10円玉にしたり、アルミニウムを缶の形にしたりと
金属結晶は伸ばしたり開いたりできるという性質があります。
これを科学用語で展性とか延性があるといいます。
こちらでも展性、延性について解説しています。
・金属結晶の特徴についてわかりやすく解説
遷移金属の性質
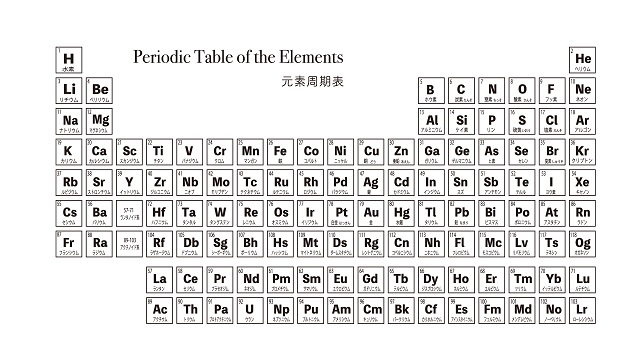
それから周期表の真ん中あたりに遷移金属(遷移元素)があります。
Fe(鉄)やCu(銅)が遷移金属です。
遷移金属はNa(ナトリウム)と比べると自由電子の数が多いという特徴があります。
自由電子は周りをくっつけるノリみたいな性質があります。
だから自由電子というノリが遷移金属に多いということは
遷移金属はガッチリへばりついているということです。
ガッチリへばりついているということは
ドロドロに溶かすのに他の元素よりもエネルギーが必要だということです。
ということで遷移金属は『融点がすごく高い』という特徴があります。
たとえばFe(鉄)の融点は約1600℃です。
すごい高温ですね。
溶鉱炉では1年くらいかけて昇温していきます。
1回火を入れたらずっと10年くらい操業し続けます。
溶鉱炉の中は千数百度になります。
通常、私たちが生活しているところで
千数百度の世界に出会うことはないでしょうけど、
それくらい鉄って融点が高いって言いたいだけです。
これに対して同じ金属でも融点が低いものがあります。
水銀Hgは融点が低いです。
 水銀の体温計
水銀の体温計今はあまり使われていませんが
体温計に水銀がよく使われていました。
液体の金属です。
水銀は金属なのに部屋の温度で液体なのです。
面白い金属ですね。
以上で金属結晶の性質についての解説を終わります。















