今回の記事では金属結晶の特徴についてわかりやすく解説していきます。
Contents
金属結晶を作る金属結合とは?
10円玉というのは銅原子(Cu)がたくさん集まってできた固体です。
5円玉貯金はアリなのか? 銅価格高騰で「50年後はレアメタル」になる可能性も https://t.co/LbAZc7aoa8
銅が高騰しているのなら10円玉でしょ、銅が95%で残りの5%は亜鉛とスズですからね。5円玉はオシャレかも知れないけど、銅に着目するなら絶対10円玉だね。— u-tan (@rakudanoojichan) June 4, 2022
金属原子がいっぱい集まると
金属の固体ができあがります。
ではどうして金属原子は集まるのでしょう?
基本的には物質というのは放っておくとバラバラになろうとします。
これをエントロピー増大の法則といいます。
このエントロピー増大の法則に抗う(あらがう)ための工夫が結合です。
集まるというのことは何かしら結びつくための工夫や仕組みが必要になります。
くどいようですが、基本は放っておいたらバラバラに離れていくからです。
だから以前解説した分子間力も
分子同士を結び付けるための引力です。
金属原子同士を結び付けるための引力もあるわけです。
この結びつきのことを金属結合といいます。
今回の記事のテーマである金属結晶は金属結合でできた固体のことです。
金属の例としてアルカリ金属の代表例であるナトリウムで考えてみましょうか。

上記図はナトリウム原子同士が接触して並んでいるところです。
金属の原子というのは隣り合っている部分と互いに接触する形で並んでいます。
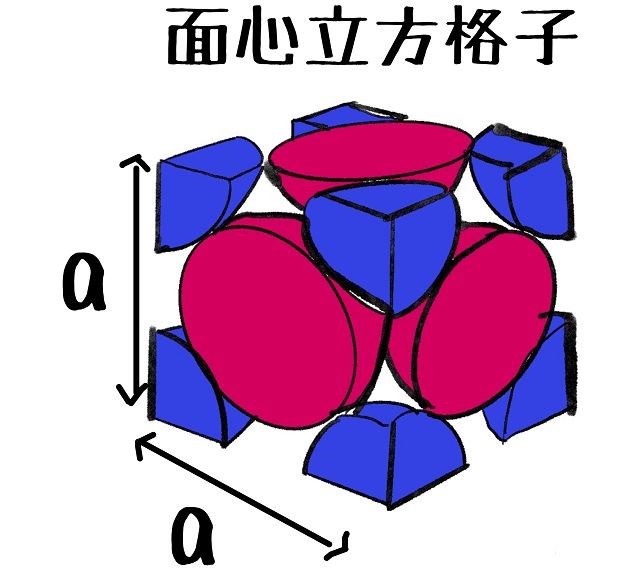
ナトリウム原子は面心立方格子なので上記図のような形でもあります。
こんな感じで接触して並んでいます。
ここでは接触しているということがわかればOKです。

こんな感じで原子同士が接触してできているわけですが、
周りに電子殻があります。
電子殻が一部接触する形で並んでいます。

ところで電子殻にはマイナスの電気を持った電子が飛んでいます。
実際には電子軌道の中に入っていますが。
とにかくマイナスの電気を持った電子($e^{ー} $)が
グルグル飛ぶにしても接触している部分を利用すれば
いろんな場所(まったく別の原子の電子殻)に飛んでいけますよね。
電子は1個の電子殻だけをグルグル回るだけではないってことです。
金属の固体の中は
電子が自由自在に動き回れる環境になっています。
こういう自由自在に動き回れる電子のことを自由電子といいます。
自由に動くから自由電子です。
ところで金属の原子は電子を失ったらどうなるでしょう?
自分が持っていた電子がどこかに行ってしまうということです。

原子が電子を失った時にはプラスの電荷をもつ陽イオンになります。
金属の固体の中では金属原子は正電荷(陽イオン)の状態になっていると考えることができます。

プラスの電気を持っている$Na^{+} $のところに
マイナスの電気を持っている$e^{ー} $がやってきたらどうなるでしょう?
プラスとマイナスで引きあう力が働きます。
これが金属結合です。
陽イオンのプラスと自由電子のマイナスの間に働く静電気的な引力が金属結合の正体です。
この金属結合によって金属原子がたくさん集合すると
金属の固体が完成します。
これが金属結晶です。
電子を失ってプラスの電荷を持った陽イオンとマイナスの電荷をもつ電子の間に
働く静電気的な引力のことを金属結合といい、
その金属結合によって原子が無数に集まると金属結晶という固体ができあがります。
ではここからが本題です。
金属結晶にはどんな特徴があるのでしょう?
金属結晶の特徴(1)電気・熱伝導性
金属には電気や熱をよく通すという性質があります。
このことを電気伝導性、熱伝導性が高いといいます。
・電気伝導性、熱伝導性が高い

マイナスの電気を持った自由電子が動くわけです。
電気伝導性というのはプラスとかマイナスの粒が動くかどうかで決まります。
マイナスの自由電子が自由に動くわけですから金属結晶には電気伝導性があります。
分子結晶に電気伝導性があるかどうか知りたい方はこちら
・分子結晶に昇華性や電気伝導性はあるの?理由とともにわかりやすく解説
あと自由電子は熱も運んでくれます。
そのため、金属結晶は熱伝導性も大きくなります。
金属結晶の特徴(2)展性、延性がある
金属結晶には展性や延性という性質があります。
展性は展開の『展』ですね。
『展』には『広がる』という意味があります。
延性は延長の『延』ですよね。
延びるということですね。
・叩いて薄く広がるという展性
・引っ張って引き延ばせるという延性
簡単にいうと金属結晶は『変形が可能』ということです。
金属結晶に展性、延性があるのはなぜ?
どうして金属の固体は叩いてもバキバキに破壊されず
変形してしまうのでしょう?

金属結合において自由電子が動き回っている状況から
想像することができます。

たとえばハンマーなんかで力が加わったとしましょう。
すると配列がずれます。
ただ、金属結合において金属の原子同士をつなぎとめているのはある意味自由電子です。
自由電子が接着剤のような働きをすることで結びついています。
でも、自由電子という接着剤は自由に動けます。
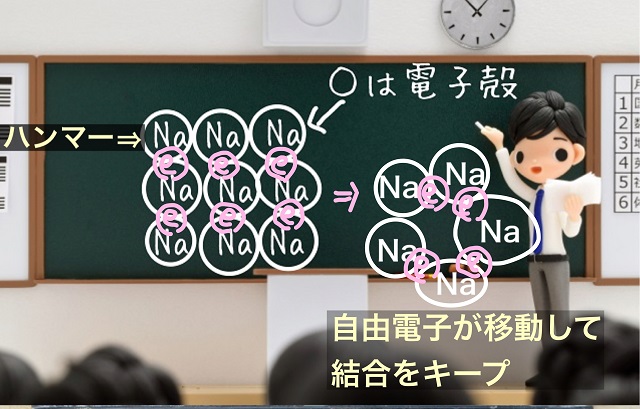
ということはたとえ原子の配列がずれたとしても
原子同士の接触さえしてくれていれば
接着剤である自由電子が移動して結合がキープされます。
そうやって金属結合という結合をキープすることができるわけですね。
こんな感じでハンマーで叩くなどした結果、
配列がズレたとしても。結合が途切れません。
これが金属結合に展性、延性という性質がある最大の理由です。
配列がズレたとしても接触さえしてくれたらOKということですね。
その接着剤の役割を担うのが自由電子です。
原子の配列が仮にズレたとしても
自由に動ける接着剤の役割を担う自由電子が移動することにより
金属結合が途切れないから。
金属の中で展性、延性という性質が一番強いものは?
金が一番強いです。
金は展性、延性が一番大きいです。
どれくらい展性、延性が大きいでしょう?
|
|
コチラは物価によりだいぶ価格は変動しますが金1gです。
ハンマーでバンバン叩いていきます。
するとどれくらいの金箔を採取できるでしょう?

1gの金から畳半畳分くらいの金箔を作ることができます。
ものすごい展性ですよね。
ちなみに銀は金に次ぐ展性、延性の強さがあります。
あと、引っ張って伸ばすという延性という性質も金が最大ですが、
1gの金から金の糸を3000m分も作ることができます。
以上で金属結晶の特徴に関する解説を終わります。