「ナトリウムの最外殻電子数はいくつだったっけ?」
みたいな感じで最外殻電子数の問題を得点源にできていない学生は多いです。
という私もかつてそうでした。
⇒当ブログ管理人のプロフィール
電車で隣の大学生がなにやら塩素原子の最外殻電子数の問題を解いているのが見える
懐かしいなと思いながらも何かスマホで調べ物をしているようで、そんなもん即答やろとも思ってしまう— Altair (@altairicerca) June 4, 2020
そこで今回の記事では最外殻電子数の求め方について
問題を使ってわかりやすく解説していきたいと思います。
Contents
最外殻電子数の求め方
最外殻電子数の求め方を理解するために
以下の問題を一緒に解いていきましょう。
以下の2つの原子の最外殻電子数の和はそれぞれいくらですか?
・NとB
・LiとF
・AlとMg
・OとBe
・SiとC
この手の問題はこれから解説する内容を理解し覚えておけば
めちゃくちゃ簡単に感じれるようになりますからね。
頑張ってついてきてくださいね。
最外殻電子数の問題が解けるようになるには
周期表の暗記はマストです。
といっても、原子番号20番までで十分です。
水兵リーベぼくの船。なまがりシップスクラークか。
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
・水兵リーベ・・・水兵のリーベさん
・ぼくの船・・・水兵リーベさんの船という意味
・なまがり・・・七曲り、七回曲がるという意味
・シップス・・・船
・クラークか・・・クラークさんか!
あとは同族元素(周期表の縦)も語呂合わせで暗記しましょう。
同族元素同士は性質が似ているので、いろんな問題に対応しやすくなりますよ。
まず、周期表は語呂合わせで覚えましょう。
化学。パート1
まずは、周期表を覚えてください。
なぜなら、テスト範囲に書いた通り、族と周期の問題が出ます。
なぜなら、周期表から最外殻電子の数が機械的に分かります。最外殻電子の数は 次の『電子式』に繋がります。 pic.twitter.com/yvsE8uQdIp— Shimoyama (@Hi_Shimoyama) October 13, 2015
以下は原子番号20番まで語呂合わせで暗記した前提で解説していきますね。
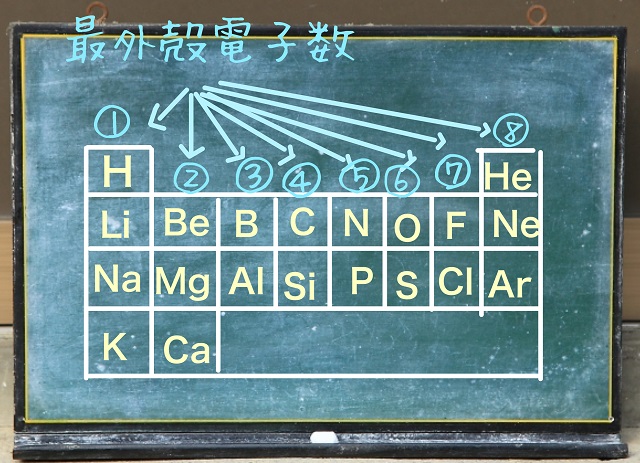
最外殻電子というのは縦の列(同族元素)のことです。
なので、上記表のようになります。
・H(水素)
・Li(リチウム)
・Na(ナトリウム)
・K(カリウム)
で、最外殻電子数は1です。
・Be(ベリリウム)
・Mg(マグネシウム)
・Ca(カルシウム)
で、最外殻電子数は2です。

上記表の見方がわかりましたか?
たとえばC(炭素)の最外殻電子数は4つですよ。
大丈夫ですか?
以上を踏まえた上で、さっきの問題を一緒に解いていきましょう!
以下の2つの原子の最外殻電子数の和はそれぞれいくらですか?
・NとB
・LiとF
・AlとMg
・OとBe
・SiとC
・NとBは最外殻電子数がNが5でBが3なので5⁺3=8個
・LiとFは1+7=8個
・AlとMgは3+2=5個
・OとBeは6⁺2=8個
・SiとCは4⁺4=8個
です。
これで最外殻電子数の問題が解けるようになったと思います。
最外殻電子数と価電子数の違い
最外殻電子数の問題が解けるようになったら
つぎは試験に出題されたら頭が真っ白になりやすい知識も整理しておきましょう。
私には高校生の娘がいるのですが、
少し前、中間テストの勉強で「価電子と最外殻電子の違いがわからない」と悩んでいました。
原子に存在する電子って電子殻に収容されています。

ちなみにイメージとして覚えておいて欲しいのですが、
原子核が中心にあって、その周りに電子が存在している感じです。
電子たちは電子殻というエリアに存在していて
原子核に近い側からK殻、L殻、M殻・・・
みたいになっているってことです。
だから原子核は電子殻ではありません。
電子殻はK殻とかL殻の話ですからね。
中心にある原子核から外側に向かって K殻・L殻・M殻となっていますが、
それぞれの原子の一番外側の電子殻(LiならL殻)にある電子数が最外殻電子数(Liなら1個)です。
これに対して価電子数は『化学結合に関係する』電子数のことです。
基本的に化学結合に関係する電子というのは最外殻電子です。
たとえばNaClは最外殻電子が1個のNaと最外殻電子が7個のClが結合してできます。
だからNaの最外殻電子数も価電子数も1でClの最外殻電子数も価電子数も7です。
でも、Ar(アルゴン)とかHe(ヘリウム)みたいな希ガスって
安定していて化学結合しません。
だからたとえばArの最外殻電子は8ですけど、化学結合しないので価電子数は0となります。
まとめ
・最外殻電子は電子殻の一番外側に存在する電子数(Naなら1個)
・価電子は化学結合するときに関係する電子数で
原則は価電子=最外殻電子だけど希ガスは例外
・希ガスは価電子が0となる
以上で解説を終わります。















