前回の記事ではボルタ電池の仕組みと欠点について解説しました。
⇒ボルタ電池の仕組みと欠点についてわかりやすく解説
今回の記事ではボルタ電池の知識を前提に
濃淡電池の仕組みと反応式についてわかりやすく解説していきます。
濃淡電池の反応式と仕組み
濃淡電池は高校化学の範囲を超えています。
ですが、前回解説したボルタ電池の仕組みが理解できているなら
濃淡電池の反応式や仕組みは簡単に理解できますよ。
⇒ボルタ電池の仕組みと欠点についてわかりやすく解説
さていきましょう。
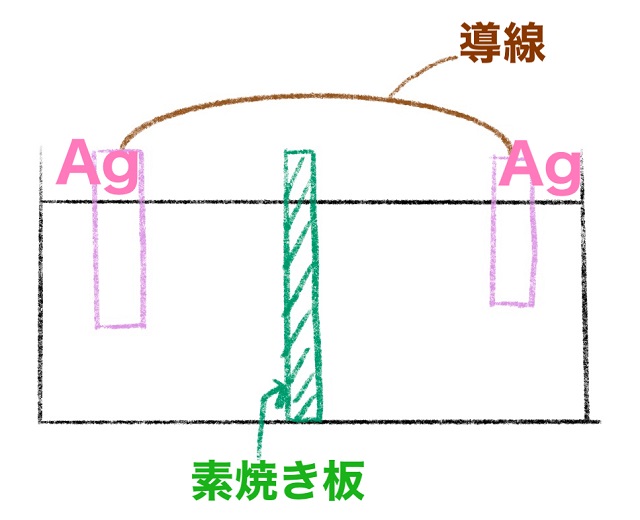
ボルタ電池と違って濃淡電池は左も右も銀(Ag)板です。
間を素焼き板で仕切ります。
素焼きってご存じですか?
縄文式土器とか弥生式土器です。
お茶漬けを作れないやつです。
昨日7月27日は、北海道・北東北の縄文遺跡群が世界文化遺産に登録されて1周年!
五所川原市某所で、縄文土器風の素焼きの鍋🍲で、縄文鍋に挑戦してみました。
食材はほぼ地物を用意して直火🔥調理。あえて塩🧂だけで自然の滋味を引き出しました😊#奥津軽 #縄文 #津軽半島 #土器 #世界遺産 #jomon pic.twitter.com/R4LNBMbgqw
— 青森県西北地域県民局 (@seihokuarea) July 28, 2022
ご飯入れてお茶入れても漏れてしまうのが素焼き。
染みるってことです。
素焼き板は染みないとダメです。
電気が流れませんからね。
この時期植物の植え替えしたらいけないんだけど、前に買った鉢底穴開いてなくて植物たちが枯れ始めたから慌てて植え替え😂
素焼きの鉢って水分染みるのね
ヴィンテージというか普通にボロい鉢みたいになってしまった…
— あ (@ao_u2) February 18, 2021
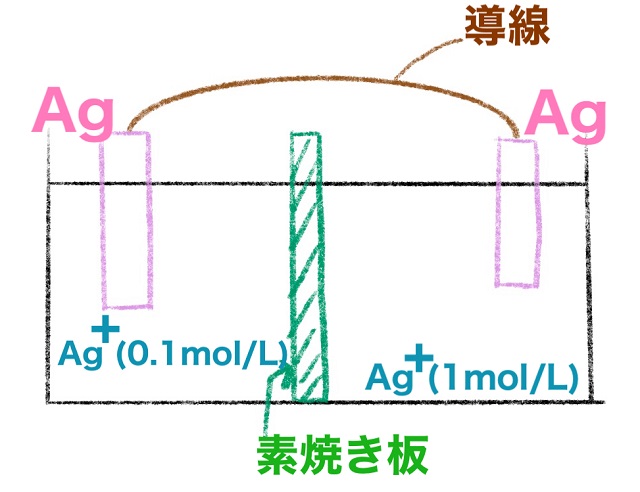
そして両方に硝酸銀を入れます。
液体の中に入るので銀イオン$Ag^{+} $の状態です。
よくわからないか方は電離の記事をご覧ください。
こちらです。
⇒電離度覚えるべきもの一覧と公式について解説
話を元に戻します。
左も右も銀イオン$Ag^{+} $が入っています。
ですが、左と右とでは濃度が違います。
ここでは左側が0.1mol/Lで右側が1mol/Lとしましょう。
本質的には右側の方が濃度が濃いですよって理解で十分です。
濃度が違わないと『濃淡』電池ってなりませんからね。
左も右も濃度が同じだと何も起こりませんからね。
だって左も右もどちらも同じ銀イオン$Ag^{+} $ですからね。
・左も右も溶液の種類はまったく同じ
・濃さだけが違う
電池のことです。
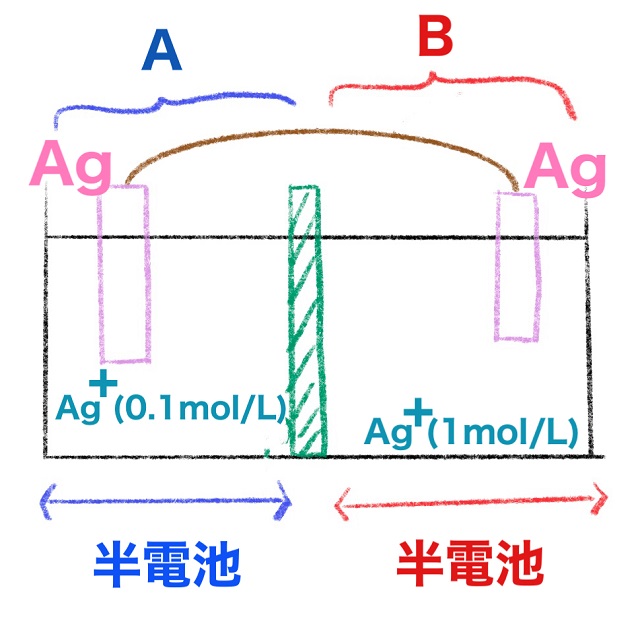
ところで左半分だけ、
銀イオンが溶けていてそこに銀板を差し込んだもの、
これを半電池(はんでんち)といいます。
そして右半分も銀イオンが溶けていてそこに銀板を指してもので
これも半電池といいます。
つまり左側の半電池と右側の半電池で一つの電池ができているわけです。
実は半電池の『半』というのは半反応式の『半』と同じ意味です。
⇒半反応式の問題を解きながら作り方も覚えよう!
半反応式と半反応式で電子を消去して
1本のイオン反応式になるというのと半電池は同じ意味ですよってことです。
半電池と半電池を組み合わせると1個の電池ができるって話です。
くどいようですが、銀イオンに同じ種類の銀板を差し込んだもの。
これを半電池といいます。
銀イオンが溶けていたら銀を挿すってこと。
これが半電池です。

説明しやすくするために
左半分をA、右半分をBにして考えていきましょう。
ところで濃度が違ったらどうなるでしょう?
濃さが違うと同じ濃さになろうとします。
濃度が違ったら同じ濃度になるように反応するということは
イメージできますよね!?
Aの方が0.1mol/LとBの1mol/Lと比べて薄いから
Aは濃くなろうとします。
つまりAの銀イオン($Ag^{+} $)が増えるのです。
$Ag $⇒$Ag^{+} $+$e^{ー} $
となります。
また$Ag^{+} $が増えるということは
Aの銀板が溶けるということです。
銀板の銀が溶けることによって銀イオンが供給されるということです。
それからB。
BはAと比べて濃いですよね。
濃いから薄くなろうとします。
薄くなるということは銀イオンがBの銀板に戻っていくということです。
銀イオンが減っていくということ。
だから
$Ag^{+} $+$e^{ー} $⇒$Ag $
となります。
ということで
A,Bそれぞれで
A:$Ag $⇒$Ag^{+} $+$e^{ー} $
B:$Ag^{+} $+$e^{ー} $⇒$Ag $
という反応が起こるということです。
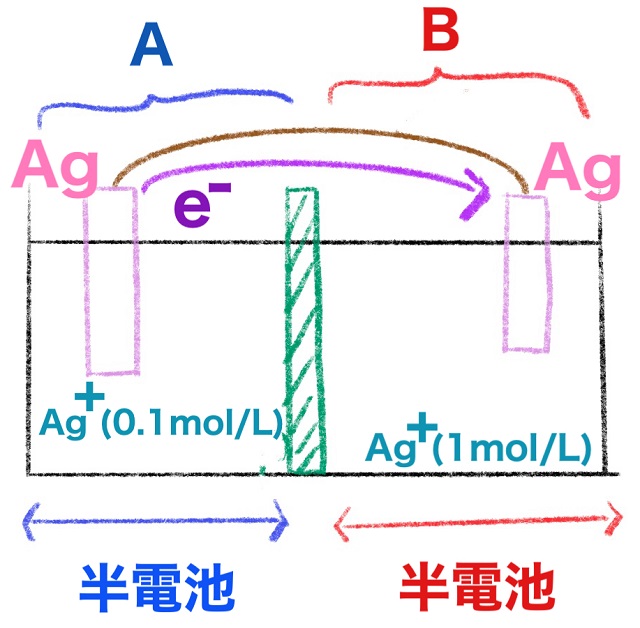
ここからが重要です。
A:$Ag $⇒$Ag^{+} $+$e^{ー} $
B:$Ag^{+} $+$e^{ー} $⇒$Ag $
という反応からBに電子が入りました。
Aからは電子が出ています。

ということは電子はAからBに移動するってことです。
(上の図の紫色の部分を参考にしてください)
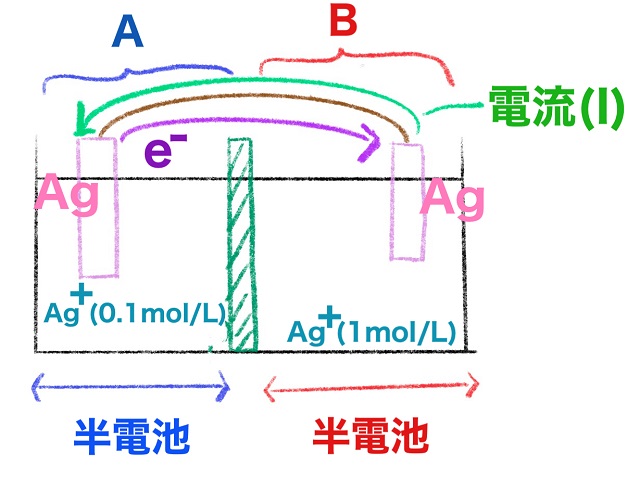
そして前回解説したように電流は電子の向きと逆向きになります。
⇒ボルタ電池の仕組みと欠点についてわかりやすく解説
つまり右から左に(BからAに)電流(I)は流れるということです。
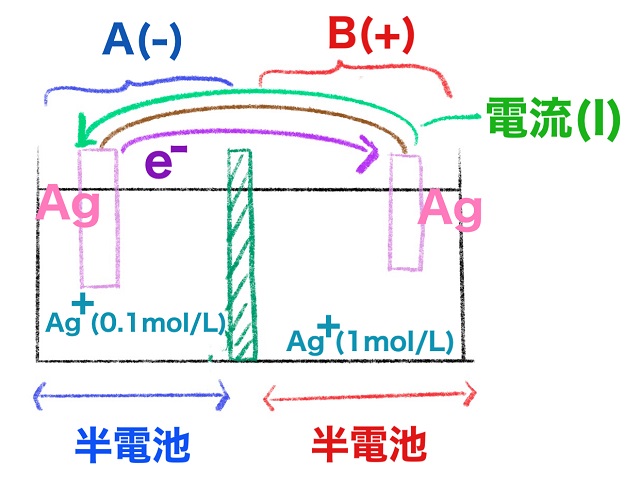
電流は電池のプラスから出ます。
そしてマイナスに入ります。
だからBがプラス、Aがマイナスになるということです。
こうやって理屈が分かっていれば
濃淡電池も導くことができます。
こんな感じで濃淡電池は濃度差だけでできます。
以上で解説を終わります。















