この記事では酸と塩基の見分け方について解説していきます。
が、まず酸や塩基って何なのでしょう?
まずその辺から解説していき、
記事の後ろの方で酸と塩基の見分け方について解説していきます。
なので、酸と塩基の見分け方だけを知りたい方が、
記事の後ろの方に移動してくださいね。
酸の性質(塩基との見分け方としても重要)
まず中学校の復習から入っていきます。
どんな性質を持ったものを酸というのか、
どんな性質を持ったものを塩基(アルカリ)っていうのでしょうか?
まず、酸の性質から。
酸って舐めるとどんな味がしますか?
酸っていう漢字は『酸(す)っぱい』と『す』と読めますね。
実際、酸は酸っぱいです。

だから梅干し、レモンの汁とかお酢などは酸の仲間です。

他にも炭酸も酸っぱいのですが、
いろいろな甘味料が入っているので
酸っぱいという味よりも爽快感が出ています。
でも、炭酸だけだったら酸っぱい味がします。
酸の性質として共通する味覚に対する影響としては
『酸っぱい』という影響があります。
これは酸の水素イオンが舌を刺激して
酸っぱいという味覚を人間に与えているから起こる現象なのです。
酸っぱいという味覚に対する性質が酸にはあるということです。
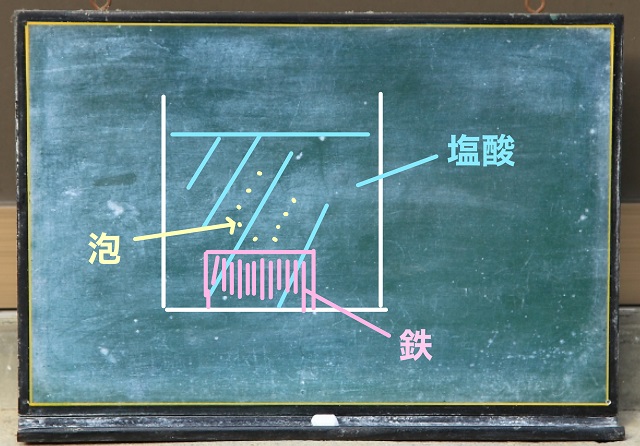
それから、たとえば、塩酸が入った容器に鉄を入れたとしましょう。
すると、鉄が溶けることで泡が出ていきます。
こんな感じで酸は金属を溶かすという性質もあります。
あとリトマス紙。
青色のリトマス紙を酸は赤くする性質があります。
青色リトマス紙を赤く変色させるのが酸の性質として有名です。
リトマス紙の変色の覚え方としては『ルパン三世』があります。
ルパン三世の三世を『酸性』と読み替えます。
/
カラオケルームでアニメ鑑賞!
『 #ルパン三世 the Last Job』を#JOYSOUND「みるハコ」で無料配信!
\📅1月19日(水)〜4月18日(月)https://t.co/55iUTPzgUr
対象機種「JOYSOUND MAX GO」を導入の全国のカラオケルームにて無料(別途室料)で楽しめる!@JOYSOUNDshop @lupin_anime pic.twitter.com/eUriiWJ9K9
— Filmarks【アニメ】 (@Filmarks_anime) January 16, 2022
で、ルパン三世は赤いジャケットを着てますよね。
昔は青色のジャケットでした。
━━━━━━━💰#アニロク 放送情報
💰━━━━━━━今夜の #アニメ26 は!
26時~
ルパン三世 PART1
#13 タイムマシンに気をつけろ!お楽しみに✨#ルパン #アニメ#BS12 トゥエルビは全国無料放送📺https://t.co/wQA2H1772Z
— BS12アニメ公式 (@BS12_anime) January 26, 2022
つまり昔のルパン三世のジャケットは青色でその後赤色になる。
で、ルパン三世の三世を酸性と置き換えたら
リトマス試験紙の前後(青色が赤色になる)の色の変化と同じことから
リトマス試験紙の色の変化の覚え方として有名です。
あと、酸はpHが7よりも小さいです。
まとめますと、
・酸っぱい(味覚)
・金属を溶かす
・青色リトマス紙を赤色にする
・pHが7より小さい
などがあります。
これらの酸の性質は当然ですが、
塩基との見分け方としても重要です。
たとえばリトマス試験紙を青色から赤色に変えないなら
それは酸ではありませんからね。
塩基(アルカリ)の性質(酸との見分け方としても重要)
塩基やアルカリっていったい何でしょう?
塩基とアルカリの違いですが、アルカリは水溶液の状態を言います。
これから解説する性質を持っている水溶液をアルカリといいます。
水溶液でないもの(固体や液体)を含めて塩基といいます。
さらに詳しい解説はこちらをご覧ください。
⇒アルカリと塩基の違いをわかりやすく解説
⇒アルカリとは何か?種類とともわかりやく解説
なので、アルカリを含むのが塩基なので塩基という用語で説明を続けますね。
では塩基の性質としてどんなものがあるでしょう?
まず一番大きいのが、ここまで解説してきた酸の性質を打ち消す働きがあります。
・酸っぱい(味覚)
・金属を溶かす
・青色リトマス紙を赤色にする
・pHが7より小さい
でしたね。
なので塩基は上記酸の性質を打ち消す作用があります。
たとえば、酸っぱい性質がなくなるとか、
金属が溶ける性質がなくなるとか、
青色リトマス紙を赤色に変える性質がなくなるなどの性質を持ったものを塩基といいます。

あるいはそれ以外に塩基には
赤色リトマス紙を青くする性質があります。
あとはpHが7より大きいです。
・酸の性質を打ち消す作用
・赤色リトマス紙を青くする
・pHが7より大きい
があります。
ここまで酸や塩基の性質を『具体的に』説明してきました。
では酸や塩基を見分けるための共通的な考え方について説明していきます。
酸・塩基の見分け方
アレニウスの定義とブレンステッドの定義があります。
これらの人は酸や塩基に見られる共通性質を見出し、
定義化しました。
アレニウスの定義は水に溶けて$H^{+} $を出すのが酸。
塩基は水に溶けて$OH^{ー} $を出すものをいいます。
こういった物質にここまで解説してきた酸や塩基の性質が見られたと
アレニウスさんは発見したのです。
ただ水に溶けてないものもありますね。
たとえば水酸化ナトリウムの固体とかアンモニアの気体は
水に溶けた状態ではありません。
いつも水に溶けたものばかりではありません。
塩化水素という気体だって存在します。
水に溶けたものはアレニウスの定義で対応できます。
でも水に溶けてないものはうまくいきません。
そこで範囲を広げようということで登場したのがブレンステッドの定義です。
ブレンステッドの定義では
酸とは$H^{+} $を相手に与える物質で
塩基は$H^{+} $を相手から受け取る物質のことです。
つまりブレンステッドは水素イオンの受け渡しにフォーカスして定義しました。
こうすることで、固体や気体に対しても酸や塩基の定義ができます。
結果、酸と塩基を受験問題で見分けることが可能になります。
ブレンステッドの定義で酸、塩基を見分けてみましょう。
以下の化学式をご覧ください。
$HA $+$H_2O $⇒$A^{ー} $+$H_3O^{+} $
ここで$H^{+} $の移動方法にだけ注目してください。
どこからどこに$H^{+} $が移動しているでしょう?
上記化学式では$HA $にある$H^{+} $が$H_2O $に移動しています。
だから結果、右側では$A^{ー} $と$H^{+} $を失い、
$H_3O^{+} $と$H^{+} $をもらっているわけです。
だから$H^{+} $は$HA $から$H_2O $に移動したことがわかりますね。
与えるものが酸で、受け取るものが塩基です。
$H^{+} $をサッカーのPKだとしたら
ボールを蹴る人が$H^{+} $で受け取るキーパーが塩基です。
なので、$HA $が酸で$H_2O $が塩基という風に定義できます。
これがブレンステッドの定義であり、
酸と塩基を見分ける方法になります。
$H^{+} $だけに着目して渡せば酸、もらえば塩基と定義します。
こうすれば、水溶液以外の物質でも酸と塩基の区別ができるようになります。
以上で解説を終わります。
酸と塩基については以下の記事でも解説していますので
興味のある方はご覧ください。
⇒酸と塩基の強弱って何が違う?
⇒アルカリと塩基の違いをわかりやすく解説
⇒酸とは何?わかりやすく解説